SEMEIOTICA RADIOLOGICA E SCALE DI VALUTAZIONE DELL’ARTROSI IN RADIOLOGIA CONVENZIONALE
AUTORI:
1Fausto Salaffi, 2Marina Carotti,
1Clinica Reumatologica Ospedale “Carlo Urbani”, Dipartimento Scienze Cliniche e Molecolari Università Politecnica delle Marche, Jesi, Ancona
2Radiologia Generale e Pediatrica – Dipartimento di Scienze Radiologiche, Università Politecnica delle Marche, Ancona
Introduzione
L’artrosi rappresenta una delle principali cause di dolore e di disabilità (Nelson AE et al. Semin Arthritis Rheum. 2014 – Salaffi F, et al. Aging Clin Exp Res. 2005 – Salaffi F, et al. Clin Rheumatol. 2005 – Salaffi F, et al. J Rheumatol. 1991). A tutt’oggi, nonostante le più moderne tecniche di imaging, la radiologia tradizionale resta una tecnica fondamentale ed irrinunciabile nello studio dell’artrosi (Braun HJ, et al. Bone. 2012), non solo per l’identificazione delle lesioni elementari (riduzione della rima articolare, osteofiti marginali, sclerosi subcondrale e cisti) e dell’entità del danno anatomico, ma anche per la valutazione della progressione radiologica nel tempo e l’indentificazione dei fattori predittivi di progressione radiologica (Nieminen MT, et al. Osteoarthritis Cartilage. 2019 – Sakellariou G, et al. Ann Rheum Dis. 2017). Come per l’artrite reumatoide, anche per l’artrosi sono stati proposti e validati numerosi metodi di scoring radiologici semiquantitativi per la valutazione della progressione del danno anatomico. Essi comprendono scale che prevedono una valutazione globale del danno articolare e scale in cui le singole lesioni evidenziate radiologicamente vengono punteggiate separatamente. Sia negli studi epidemiologici che nei trial clinici, allo scopo di ottenere misure affidabili, utili allo studio della progressione radiologica in radiologia convenzionale, è indispensabile attenersi a procedure standardizzate, riconducibili alla tecnica radiologica (inclinazione del fascio di raggi X), al posizionamento del paziente, alla sede di misurazione, al metodo di misurazione, nonché al training del lettore o il numero dei lettori (Mathiessen A, et al. Best Pract Res Clin Rheumatol. 2016).
Alterazioni radiologiche elementari in radiologia convenzionali
I segni radiologici caratteristici dell’artrosi consistono in una marcata riduzione della rima articolare, eburneizzazione, formazione di cisti e osteofitosi (Figura 1) (Boesen M, et al. Osteoarthritis Cartilage. 2017). Essa può essere complicata da sublussazione, disallineamento, anchilosi fibrosa e formazione di corpi liberi intra-articolari di natura ossea e cartilaginea. Tipicamente, la riduzione della rima articolare è asimmetrica e localizzata prevalentemente nelle zone articolari sottoposte a maggior carico quali lo spazio femoro-tibiale mediale del ginocchio (Figura 1).
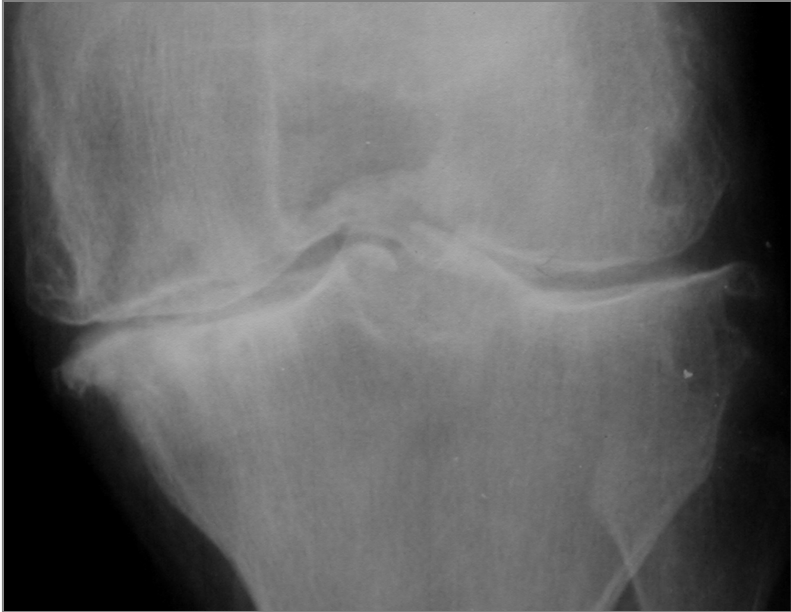
Figura 1: Gonartrosi femoro-tibiale. Riduzione della rima articolare, più rilevante nel compartimento femoro-tibiale mediale, osteofitosi marginale, sclerosi dell’osso subcondrale e cisti subcondrali
In alcune aree la riduzione della rima articolare può essere diffusa, con interessamento dell’intera articolazione (caviglia e articolazioni interfalangee della mano). In seguito alla progressiva scomparsa della cartilagine articolare, l’osso subcondrale va incontro a vari gradi di ipercellularità e di ipervascolarizzazione, evidenziabili radiologicamente con l’eburneazione ossea, per formazione di nuovo tessuto osseo sulle trabecole preesistenti. Le cisti sono di frequente riscontro nell’artrosi e sono definite in vario modo: cisti sinoviali, cisti sub-condrali, pseudocisti sub-articolari, pseudocisti necrotiche e geodi (Guermazi A, et al. Osteoarthritis Cartilage. 2014). Sul piano radiologico, si manifestano come aree radio-trasparenti circoscritte, a limiti netti e di dimensioni variabili (2-20 mm) e si distinguono dalle altre lesioni radio-trasparenti per la molteplicità, la distribuzione segmentale, la sclerosi circostante e l’alterazione di un’articolazione adiacente. Gli osteofiti sono la più tipica manifestazione dell’artrosi. L’osteofita può essere marginale (escrescenza a livello dei margini, ovvero nei siti dove la cartilagine articolare si continua con la membrana sinoviale e con il periostio, producendo degli “orli” d’osso), centrale (escrescenza a livello delle aree centrali dell’articolazione, che produce un profilo “bozzoluto”), periostale o sinoviale (ispessimento periostale con apposizione ossea) e capsulare (orli d’osso che si sviluppano nei siti d’inserzione della capsula articolare e dei legamenti articolari). Le sedi più comuni di artrosi extra-rachidea sono le articolazioni interfalangee (Figura 2) e metacarpofalangee delle mani la prima carpo-metacarpale, l’articolazione trapezio-scafoidea del polso, l’anca ed il ginocchio (Hayashi D, et al. Ann Phys Rehabil Med. 2016). A livello del rachide cervicale e lombare, invece, le articolazioni interapofisarie, unco-vertebrali e costo-vertebrali sono le sedi più colpite dall’artrosi e le alterazioni evidenziabili radiologicamente sono caratterizzate dalla presenza di osteofiti, di sclerosi ossea reattiva e dal restringimento dello spazio discale con eventuale presenza del segno del “vacuum”, ovvero di una raccolta gassosa intradiscale, evidenziabile come immagine radiotrasparente lineare o circolare (Hayashi D, et al. Osteoarthritis Cartilage. 2012).
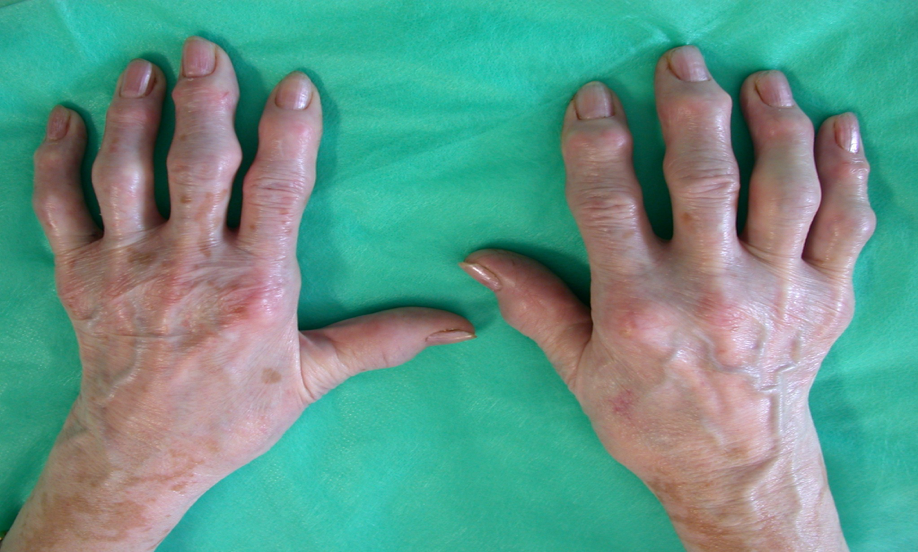
Figura 2: L’artrosi della mano si caratterizza per la formazione di tumefazioni dure a carico della superficie dorsale delle interfalangee distali, note come noduli di Heberden e delle articolazioni interfalangee prossimali (noduli di Bouchard)
ARTROSI DELLA MANO
L’artrosi della mano si caratterizza per la formazione di tumefazioni dure a carico della superficie dorsale delle interfalangee distali (IFD), note come “noduli di Heberden” (Figure 2 e 3). Tali noduli sono particolarmente frequenti nel sesso femminile e nell’età avanzata (Addimanda O, et al. Clin Rheumatol. 2017). Si manifestano con dolore e dolorabilità alla digitopressione e, talora, decorrono associati a segni locali di flogosi. Possono coesistere, sempre sul lato dorsale articolare, piccole cisti gelatinose contenenti un liquido viscoso costituito da acido ialuronico. Le articolazioni interfalangee prossimali (IFP) sono meno frequentemente interessate da tali noduli (noduli di Bouchard) che sono, generalmente, di consistenza più molliccia rispetto a quelli rilevati a carico delle interfalangee distali (Addimanda O, et al. Scand J Rheumatol. 2012). La tumefazione è, inoltre, più regolare, quasi fusiforme. Dopo la fase acuta, d’esordio, i noduli di Heberden e quelli di Bouchard possono divenire del tutto asintomatici ed evolvere verso deformità articolari (lussazioni o sublussazioni mediali/laterali) (Haugen IK, et al. Arthritis Res Ther. 2011 – Ramonda R, et al. Clin Rheumatol. 2014).
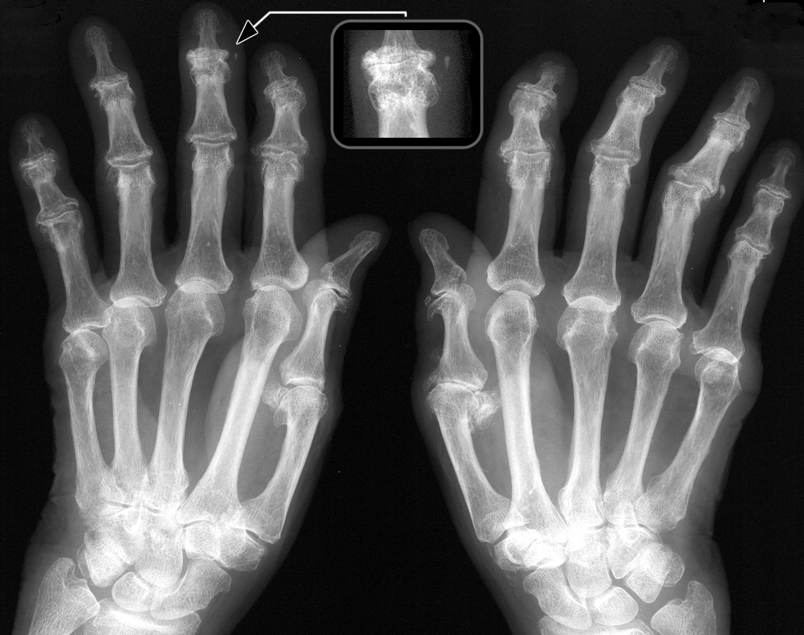
Figura 3. Evidenti manifestazioni artrosiche con osteofiti marginali a carico delle articolazioni interfalangee distali, sclerosi subcondrale e riduzione delle rime articolari
Più rara e, solitamente correlata ad attività occupazionali manuali, è l’artrosi delle metacarpo-falangee (MCF). La localizzazione artrosica a livello della trapezio-metacarpale, denominata anche rizoartrosi del pollice è frequente nel sesso femminile e si manifesta con dolore marcato alla base del pollice, acuito dai movimenti di prensione della mano o dalla digitopressione sulla faccia dorsale del pollice atteggiato in flessione, a livello della tabacchiera anatomica o sulla faccia palmare con il pollice in estensione. Nel tempo, la progressione del danno anatomico induce una progressiva deviazione della base del metacarpo fino a configurare la cosiddetta “mano quadrata” con associata deformità del pollice detto “pollice a Z” (Figura 4) (Buckland-Wright JC, et al. Osteoarthritis Cartilage. 2000).
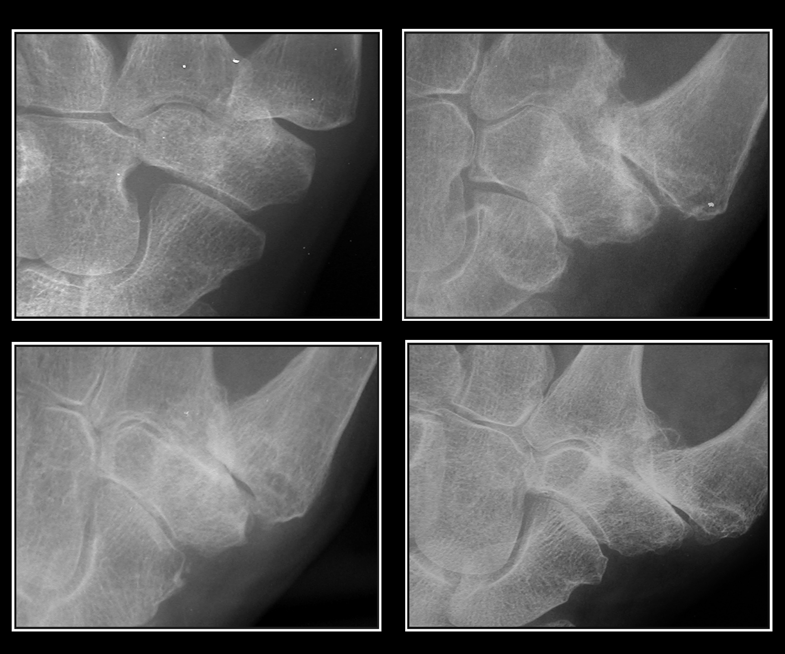
Figura 4: Interessamento dell’articolazione trapezio-metacarpale (rizoartrosi del pollice) con progressiva riduzione della rima articolare, sclerosi subcondrale e cisti subcondrali, più evidenti alla base del I° metacarpo
L’osteoartrite infiammatoria (erosiva) è considerata una variante aggressiva dell’artrosi generalizzata, anche se a tutt’oggi, non vi è accordo se essa rappresenti un’entità nosologica autonoma o se, invece, sia una forma di passaggio di una classica artrosi nodale della mano (Punzi L, et al. RMD Open. 2015). Essa colpisce, soprattutto, il sesso femminile in età perimenopausale ed ha generalmente un esordio acuto (dolore, rigidità articolare inferiore a 30 minuti, disestesie parestesie ai polpastrelli) ed una più rapida progressione del danno anatomico. I segni radiologici dell’artrosi della mano sono rappresentati dalla riduzione della rima articolare, dagli osteofiti, che possono essere anche esuberanti, dalla sclerosi subcondrale e dalla sublussazione radiale o ulnare, che determina un profilo a “zig-zag” dell’articolazione. Ai margini delle articolazioni coinvolte è possibile osservare la presenza degli “ossiculi”, che sovrastano la capsula articolare. Nell’osteoartrite infiammatoria erosiva, che coinvolge, soprattutto, le articolazioni interfalangee prossimali e distali e, in alcuni casi anche le trapezio-metacarpali, carpo-metacarpali e scafo-trapezoidi, oltre ai segni radiologici sopra indicati, si evidenziano le classiche erosioni e pseudocisti centrali, associate all’osteofitosi marginale e centrale, che realizzano l’immagine ad “ala di gabbiano” (Figure 5, 6 7) (Punzi L, et al. Best Pract Res Clin Rheumatol. 2010). L’interessamento delle articolazioni MCF si associa, in generale, a quello più marcato delle articolazioni IFP e IFD. Caratteristica è l’uniforme riduzione di una o più rime articolari metacarpofalangee. A livello del polso, è frequente il coinvolgimento dell’articolazione trapezio-metacarpale, carpo-metacarpale e di quella trapezio-scafoidea. I segni radiologici dell’artropatia degenerativa trapezio-metacarpale sono rappresentati dalla sublussazione radiale, riduzione della rima articolare, sclerosi, lesioni cistiche sub-condrali, osteofitosi e frammentazione ossea. Il coinvolgimento dell’articolazione trapezio-scafoidea è solitamente associato a quello della trapezio-metacarapale ed i segni radiologici sono rappresentati dalla riduzione della rima articolare e dalla sclerosi delle superfici contrapposte del trapezio, del trapezoide e dello scafoide (Punzi L, et al. Best Pract Res Clin Rheumatol. 2004).
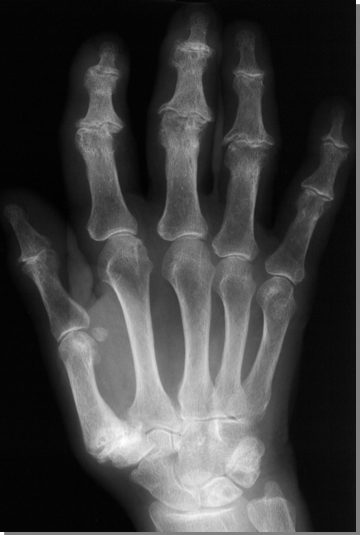
Figura 5: Osteoartrite erosiva delle mani. L’interessamento delle articolazioni interfalangee prossimali e distali e della 1° articolazione carpo-metacarpale, l’aspetto delle lesioni (osteofitosi marginale, sclerosi subcondrale, erosioni centrali “ad ali di gabbiano”) ed il modesto coinvolgimento delle articolazioni metacarpofalangee costituiscono un valido criterio di diagnostica differenziale con l’artrite reumatoide.
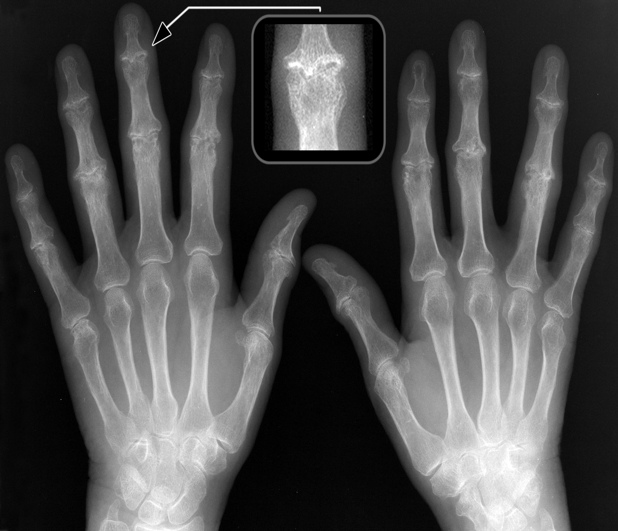
Figura 6: Osteoartrite infiammatoria erosiva. Oltre ai segni radiologici dell’artrosi nodale si evidenziano erosioni centrali ed osteofitosi centrale che caratterizzano la forma infiammatoria erosiva
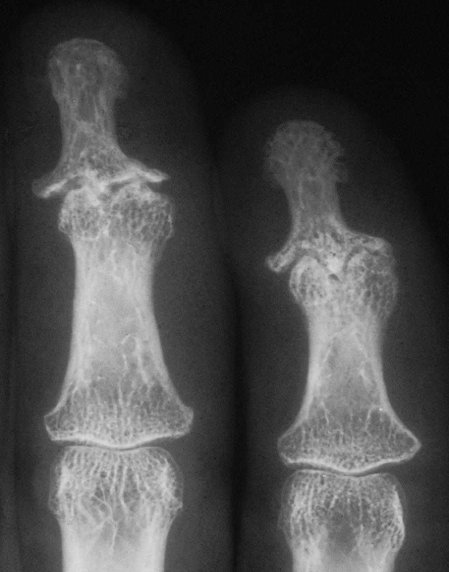
Figura 7: Osteoartrite erosiva delle mani. Interessamento delle articolazioni interfalangee distali, con osteofitosi marginale e centrale, sclerosi subcondrale, erosioni centrali, che realizzano l’immagine “ad ali di gabbiano”
L’artrosi dello spazio semilunare-capitato, è rappresentato, radiologicamente, dalla riduzione della rima articolare, dalla sclerosi e dalla formazione di cisti ed è, in genere, di natura post-traumatica. Tale anomalia si associa, frequentemente, con la diastasi scafo-semilunare e la riduzione della rima radio-scafoidea. Le corrispondenti alterazioni radiologiche sono definite collasso scafo-semilunare di grado avanzato o “polso SLAC”. È possibile osservare anche l’interessamento della radio-carpica con prevalente localizzazione a carico della radio-scafoidea (Figura 8). Sebbene la radiologia convenzionale rappresenti una tecnica fondamentale e di prima istanza nello studio dell’artrosi della mano, la risonanza magnetica si è dimostrata di particolare utilità, sia negli stadi iniziali che nelle fasi più tardive del processo degenerativo. Essa consente la visualizzazione dei tessuti molli periarticolari, della cartilagine ialina, dei legamenti, dei tendini e della membrana sinoviale, distinguendoli dall’osso corticale. Il suo contrasto naturale permette di evidenziare le alterazioni morfo-strutturali articolari, prima che possano essere evidenziate all’esame radiologico standard. Pertanto, questa tecnica non dovrebbe rappresentare un’alternativa alla radiologia convenzionale, ma un utile strumento da adottare nei casi in cui le informazioni che essa fornisce possono confermare o modificare la diagnosi e l’approccio terapeutico (Addimanda O, et al. Clin Rheumatol. 2017).
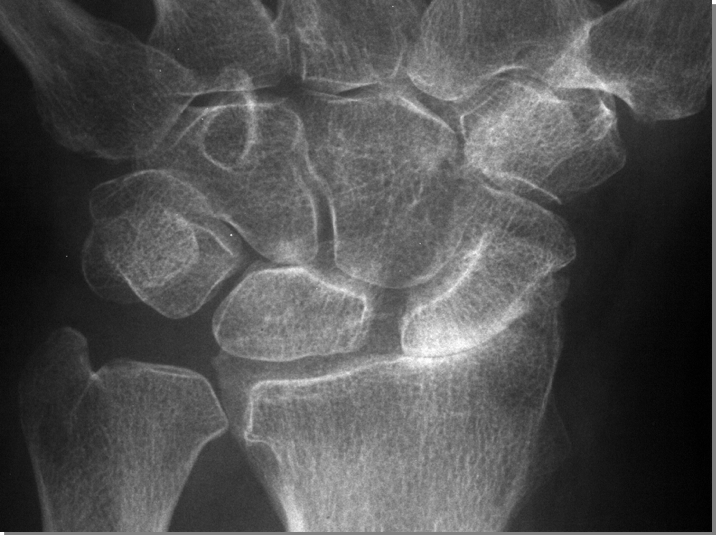
Figura 8: Artrosi primaria delle mani. Interessamento dell’articolazione radio-scafoidea, con marcata riduzione della rima articolare ed osteosclerosi subcondrale
ARTROSI DEL GINOCCHIO
L’artrosi del ginocchio (o gonartrosi) può interessare sia l’articolazione femoro-tibiale che quella femoro-rotulea. Il quadro clinico è inizialmente dominato dal dolore in sede anteriore o antero-mediale, caratteristicamente di tipo meccanico. Spesso si accompagna a contrattura dolorosa (“gelling”) che segue un’inattività prolungata e che è di breve durata, attenuandosi con la marcia (Salaffi F, et al. Reumatismo. 2014). Il dolore, nelle prime fasi, è caratteristicamente risvegliato da particolari attività (salire o scendere le scale) o posture (accovacciarsi), mentre, in seguito, può assumere caratteri di continuità, diventare notturno ed accompagnarsi a frequenti episodi di versamenti articolari (idrartro). Obiettivamente, si rileva la presenza di limitazione dolorosa dei movimenti alla flessione ed estensione forzata, scrosci articolari e dolore evocato alla digitopressione a livello dell’inserzione dei legamenti periarticolari (es. tendine della zampa d’oca). In caso di versamento articolare è opportuno eseguire un esame del liquido sinoviale che dimostra caratteristiche del liquido poco infiammatorio. Nell’artrosi femoro-rotulea si evocano crepitii e scrosci articolari inducendo uno scivolamento sagittale della rotula sul femore (segno della “pialla” o della “raspa”). Nello studio radiologico della gonartrosi occorre considerare l’articolazione come composta di tre compartimenti o spazi articolari: i compartimenti femoro-tibiale mediale e laterale ed il compartimento femoro-rotuleo. Le alterazioni sono le stesse descritte per gli altri distretti articolari e cioè la riduzione della rima articolare, la sclerosi e le lesioni cistiche subcondrali e l’osteofitosi (Rothschild BM. Ann Rheum Dis. 1992). Per lo studio della riduzione della rima articolare dovrebbero essere eseguiti radiogrammi sotto carico, in quanto la rima articolare si riduce sotto l’azione del peso corporeo. Questa tecnica consente una più accurata definizione della sublussazione del femore e della tibia e dell’angolazione in varismo o valgismo. Sebbene, a tutt’oggi non esista il metodo ideale per la valutazione, negli studi di follow-up, delle variazioni di ampiezza della rima articolare a livello dei compartimenti femoro-tibiali, le più recenti linee guida hanno proposto un metodo radiologico basato sul posizionamento del paziente in ortostatismo, con le ginocchia in leggera flessione (7°-10°), fino a venire a contatto con il film-cassetta, in proiezione postero-anteriore, con la prima metatarso-falangea in linea con il bordo della cassetta. Il raggio incidente è orizzontale ed orientato verso il centro del ginocchio (Figura 9).
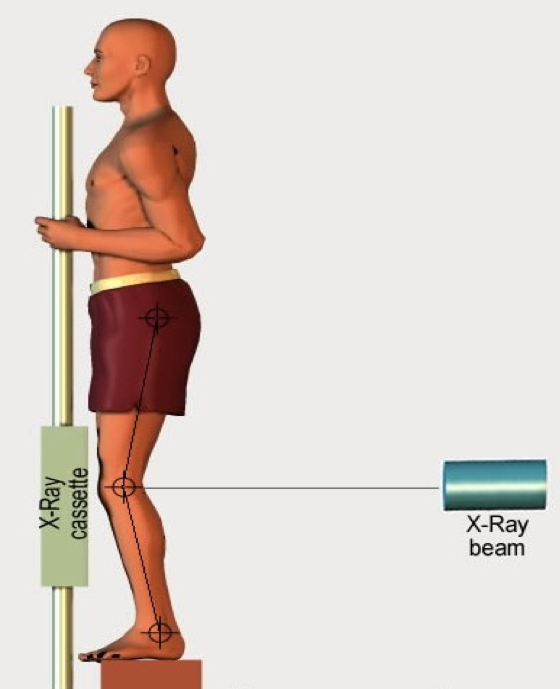
Figura 9: Studio del compartimento femoro-tibiale del ginocchio.La I MTF è posta al di sotto ed allineata alla cassetta radiografica. La rotula è a contatto con il film-cassetta ed allineata verticalmente con la I MTF. Il raggio incidente è orizzontale ed orientato verso il centro del ginocchio.
Lo studio del compartimento femoro-rotuleo richiede il ricorso anche a proiezioni oblique e tangenziali. Il coinvolgimento artrosico del ginocchio può essere monolaterale o bilaterale e, solitamente, i reperti radiografici sono più marcati nel compartimento femoro-tibiale mediale. L’interessamento monocompartimentale (compartimento femoro-tibiale mediale o, meno frequentemente laterale) o bicompartimentale (compartimenti femoro-tibiale mediale e femoro-rotuleo o, meno sovente, compartimenti femoro-tibiale laterale e femoro-rotuleo) è più caratteristico dell’interessamento tricompartimentale (compartimento femoro-tibiale-mediale, femoro tibiale-laterale e femoro-rotuleo). La riduzione della rima articolare rappresenta il segno radiologico più evidente del danno cartilagineo. Nel ginocchio, le cisti subcondrali sono meno frequenti che nell’anca. Gli osteofiti sono frequenti e predominano in corrispondenza dei margini dell’articolazione (Huch K, et al. Semin Arthritis Rheum. 1997). Il progressivo logoramento e la lacerazione dell’osso subcondrale ipervascolarizzato portano alla formazione delle fratture transcondrali. Tali fratture, di concerto con la disintegrazione della superficie articolare e la metaplasia sinoviale possono dar origine ai corpi osteocartilaginei intra-articolari o inclusi (“topi articolari”) in un sito sinoviale distante (Figura 10) (Ornetti P, et al. Osteoarthritis Cartilage. 2009).
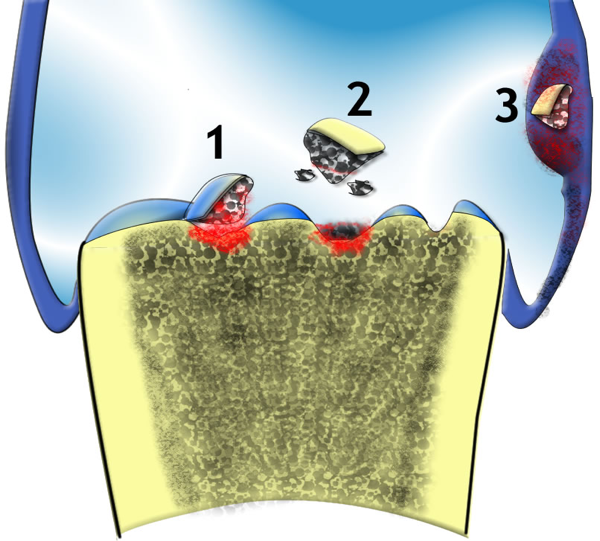
Figura 10: Corpi osteo-cartilaginei migranti (topi articolari).
Solitamente, i corpi osteocartilaginei migrano, rimanendovi incastrati, verso le depressioni dell’osso o le regioni articolari sacciformi, come l’area tibio-peroneale prossimale. Essi possono anche passare dalla cavità articolare all’interno di una cisti sinoviale confinante con la cavità stessa. Il compartimento femoro-rotuleo è frequentemente coinvolto dal processo artrosico, con le tipiche alterazioni radiografiche-patologiche (fibrillazione cartilaginea, erosioni ed eburneizzazione dell’osso subcondrale) evidenziabili a livello della superficie posteriore della rotula e della superficie anteriore del femore. Nella rotula tali alterazioni predominano sulla faccetta laterale. Solitamente, le alterazioni del compartimento femoro-rotuleo si accompagnano con quelle dei compartimenti femoro-tibiali, e più tipicamente è compromesso il compartimento femoro-tibiale-mediale. Le alterazioni isolate del compartimento femoro-rotuleo sono rare, e qualora siano presenti occorre escludere una malattia da deposizione di cristalli di pirofosfato diidrato di calcio (condrocalcinosi) (Figura 11). Le alterazioni radiologiche della femoro-rotulea sono rappresentate dalla riduzione della rima articolare (difficile da evidenziare nei radiogrammi in proiezione laterale, ma ben evidente in quelle assiali), la sclerosi e gli osteofiti, più evidenti sul versante rotuleo (Oo WM, et al. Curr Opin Rheumatol. 2017 – van Middelkoop M, et al. Semin Arthritis Rheum. 2018). Talora, a livello della corticale anteriore del femore, è possibile osservare un difetto “a scodella”, la cui patogenesi è incerta (evidenziabile anche nella malattia da deposizione di cristalli d’idrossiapatite di calcio o pirofosfato diidrato di calcio (Filippucci E, et al. Osteoarthritis Cartilage. 2009). La proliferazione ossea della superficie anteriore della rotula, espressione di entesopatia degenerativa del muscolo quadricipite femorale, provoca la formazione di escrescenze irregolari, definite “segno del dente” o “baffi della rotula”.
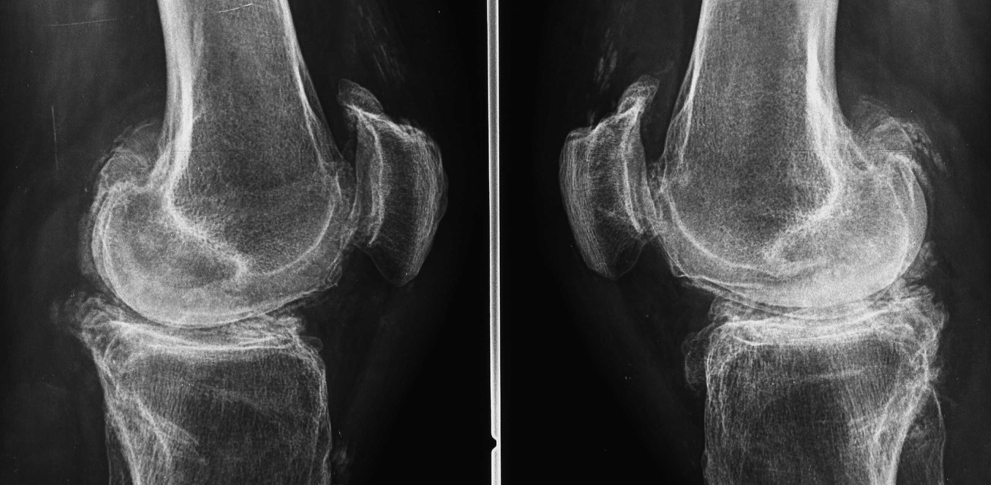
Figura 11. Tipico interessamento del ginocchio in corso di malattia da deposizione di cristalli di pirofosfato diidrato di calcio, con coinvolgimento del comparto femoro-rotuleo.
In corso d’artrosi del ginocchio la risonanza magnetica trova una particolare indicazione nelle condizioni di “discrepanza” fra i sintomi ed i reperti radiografici, per evidenziare altre possibili cause di dolore (edema osseo, osteonecrosi, lesioni interne del ginocchio) ed in studi prospettici sull’evoluzione della malattia e l’azione dei farmaci ad attività strutturale (Carotti M, et al. Radiol Med. 2017). Essa consente di rilevare lesioni non evidenziabili con altre tecniche e di valutare la composizione della cartilagine e le sue precoci alterazioni e modificazioni. L’utilizzo di sequenze appropriate consente la visualizzazione plurilaminare della cartilagine, dell’osso, dell’interfaccia osso-cartilagine e fluido-cartilagine, della membrana e del liquido sinoviale e permette di valutare le modificazioni biochimiche tessutali. La risonanza magnetica può, inoltre, accuratamente evidenziare le lesioni associate alla sofferenza cartilaginea, quali la sclerosi e le fratture dell’osso subcondrale, i piccoli geodi e le cisti, l’edema midollare, gli osteofiti e la degenerazione meniscale (più spesso interessato il mediale rispetto al laterale), frequentemente associata alla degenerazione condrale (Figura 12). Anche a livello del comparto femoro-rotuleo la risonanza magnetica consente la visualizzazione delle alterazioni morfologiche rappresentate dall’irregolarità di superficie e dalle fissurazioni ed erosioni cartilaginee, con esposizione dell’osso subcondrale, tipiche della condromalacia secondaria al processo artrosico (Figura 13) (Carotti M, et al. Radiol Med. 2017).
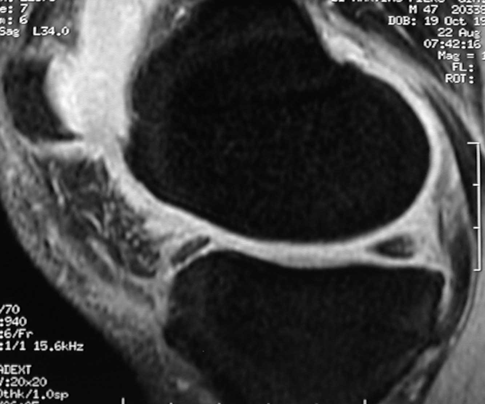
Figura 12. Gonartrosi femoro-tibiale. La sequenza Gradient Echo T2 fat-suppressed in risonanza magnetica in sezione sagittale evidenzia segni ossei di degenerazione artrosica femoro-rotulea e femoro-tibiale, con alterazione a tutto spessore della cartilagine, senza interessamento osseo subcondrale

Figura 13: Gonartrosi femoro-rotulea. La sequenza Fast Spin Echo T2 in risonanza magnetica evidenzia nella sezione assiale la fibrillazione della cartilagine, con multiple immagini lineari di iperintensità. Si associano osteofitosi della rotula, ispessimento malacico della cartilagine, sclerosi subcondrale e versamento intraarticolare di discreta entità
ARTROSI DELL’ANCA
Parimenti alle altre localizzazioni della malattia essa può essere “primaria” o più frequentemente “secondaria” a patologie congenite (displasia d’anca, coxa vara o valga), coxopatie dell’infanzia e dell’adolescenza (malattia di Perthes, epifisiolisi, ecc), turbe statiche (ginocchio varo o valgo, dismetria degli arti, scoliosi), mono- o poliartriti infiammatorie (artrite reumatoide, spondilite anchilosante, artrite psoriasica, artriti da microcristalli), morbo di Paget osseo, traumi e sovraccarico acetabolare, fratture da stress. I sintomi sono rappresentati dal dolore meccanico che può essere confinato all’inguine e/o alla regione anteriore della coscia, oppure riferito al ginocchio omolaterale (nel 25-30% dei casi), alla regione glutea o del gran trocantere. E’, inoltre, di comune riscontro la limitazione della motilità dell’anca, dapprima nei movimenti di rotazione interna e quindi in quelli di abduzione e adduzione. La deformità in flessione, più spesso tardiva, è particolarmente invalidante. Obiettivamente, si osserva un atteggiamento viziato, favorito dalla contrattura muscolare, in adduzione, flessione e rotazione esterna della coscia. Radiologicamente, l’assottigliamento della cartilagine articolare, con frammentazione, fissurazioni, erosioni, e conseguente denudazione dell’osso subcondrale, si manifesta come la riduzione asimmetrica della rima articolare (Figura 14) (Ornetti P, et al. Osteoarthritis Cartilage. 2009).
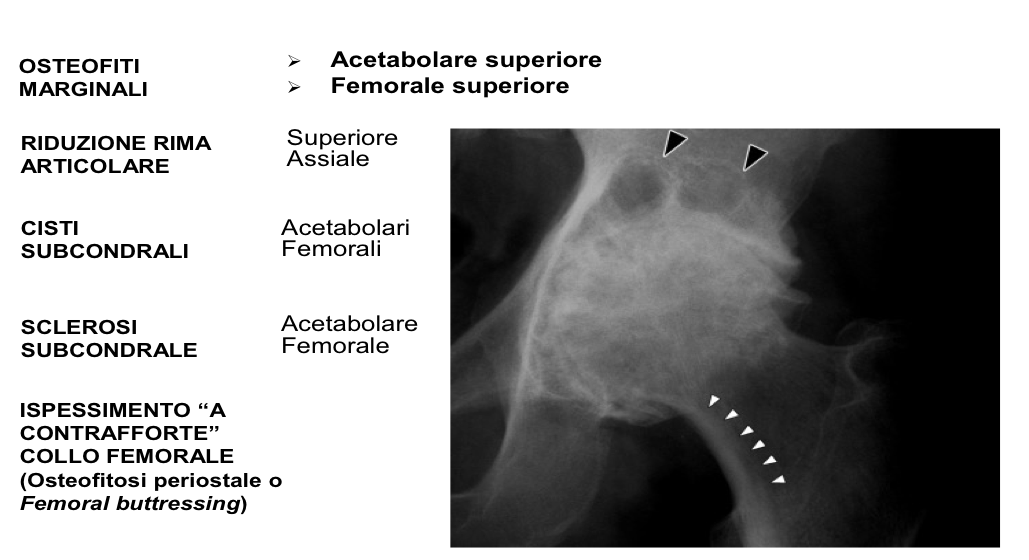
Figura 14. Principali caratteristiche radiologiche dell’artrosi dell’anca. Radiogramma in proiezione antero-posteriore con paziente in posizione supina e piedi in rotazione interna.
Caratteristicamente si rileva nelle aree soggette a maggior carico, soprattutto sul versante supero-esterno. In seguito alla riduzione o alla scomparsa della cartilagine articolare, il segmento articolare sotto pressione diviene suscettibile agli stress anomali agenti sull’osso e va incontro a collasso delle trabecole, a microfratture ed appiattimento più evidente sulla superficie portante della testa femorale. Si realizza, così, il fenomeno dell’eburneizzazione, vale a dire il deposito di nuovo tessuto osseo su trabecole preesistenti, soprattutto sulle superfici ossee strettamente contrapposte. Le cisti subcondrali sono un reperto frequente in corso di artrosi dell’anca. Abitualmente sono multiple, di dimensioni variabili (2-20 mm) e d’aspetto piriforme. Si manifestano come aree radio-trasparenti circoscritte, a limiti netti e decorrono associate con la riduzione della rima articolare e con l’eburneizzazione ossea (Lequesne MG, et al. Aging Clin Exp Res. 2003). Si distinguono dalle altre lesioni cistiche radio-trasparenti per la molteplicità, la distribuzione segmentale, la sclerosi circostante e l’alterazione di un’articolazione adiacente. Gli osteofiti sono considerati come la più tipica alterazione dell’artrosi. Essi possono avere un aspetto bottoniforme o appiattito e sui radiogrammi possono essere scambiati per corpi ossei (liberi) intra-articolari. A livello dell’anca è caratteristica l’osteofitosi periostale o sinoviale, che rappresenta la formazione d’osso a partire dal periostio o dalla membrana sinoviale. La sede più interessata da tale fenomeno è a livello della porzione mediale del collo femorale, dove è definito come “ispessimento a contrafforte” (buttressing) (Figura 15) (Siebelt M, et al. Osteoarthritis Cartilage. 2014).
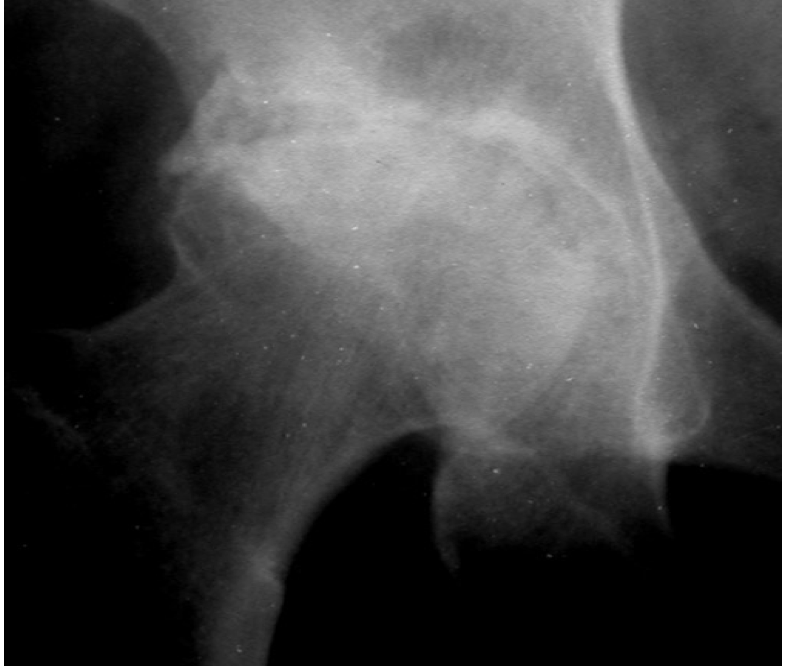
Figura 15. Coxartrosi. Riduzione asimmetrica dello spazio articolare, sclerosi e cisti subcondrali, butressing lungo il versante mediale del collo femorale.
Sul piano radiologico si distinguono tre differenti tipologie di artrosi dell’anca basate sulle posizioni reciproche della testa femorale e dell’acetabolo: a) migrazione superiore (la riduzione della rima articolare è più rilevante in corrispondenza del versante superiore dell’articolazione); b) migrazione mediale (la riduzione della rima articolare è più marcata sul versante interno dell’articolazione); c) migrazione assiale (la riduzione della rima articolare è simmetrica ed interessa tutta la cavità articolare) (Figura 16) (Sharma L. Osteoarthritis Cartilage. 2016). Nella coxartrosi, la sede più frequente di riduzione della rima articolare è il versante superiore dell’articolazione, da cui risulta la migrazione superiore della testa femorale rispetto all’acetabolo, una tipologia che può essere ulteriormente suddivisa nelle varianti supero-laterale e supero-mediale. La migrazione supero-laterale della testa femorale è più frequente nelle donne, è, di solito, monolaterale, simmetrica e può essere identificata nel 15-50% dei pazienti con coxartrosi (Siebelt M, et al. Osteoarthritis Cartilage. 2014).
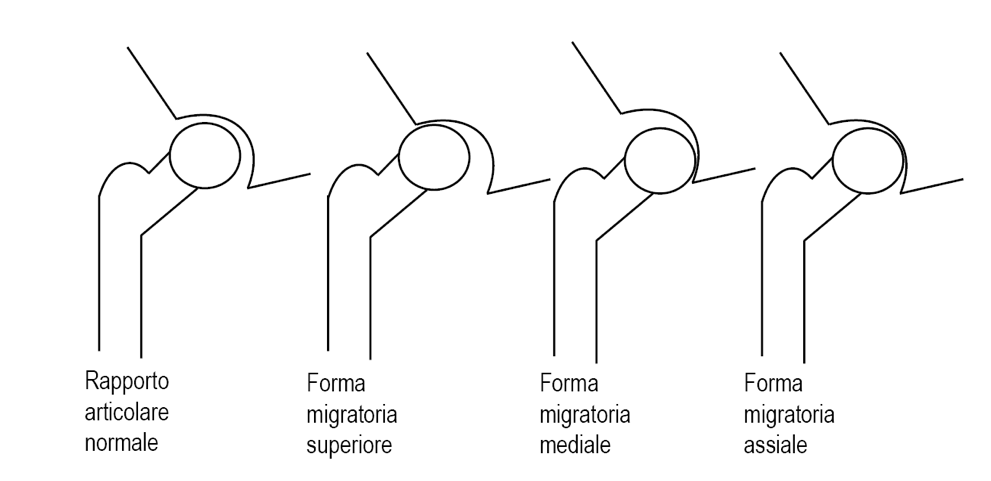
Figura 16. Differenti presentazioni radiologiche dell’artrosi dell’anca
Nella maggioranza dei casi è associata a displasia acetabolare (Figura 17). La migrazione supero-mediale della testa femorale (rilevata nel 30-40% dei casi di coxartrosi) è più frequente negli uomini ed è più spesso bilaterale. Nel 10-35% dei pazienti con coxartrosi è evidente un tipo mediale di migrazione della testa femorale che è, più spesso, bilaterale e simmetrica e predilige il sesso femminile. Il radiogramma convenzionale evidenzia la traslazione mediale della testa femorale con marcata riduzione della rima articolare mediale ed associato ampliamento di quella laterale. Possono manifestarsi deformità tipo la protrusione acetabolare. La migrazione assiale della testa femorale dovuta a riduzione diffusa e concentrica della rima articolare è infrequente. Alla presenza di tale situazione devono essere escluse una coxite isolata o secondaria ad una malattia infiammatoria cronica (artrite reumatoide, spondilite anchilosante, artrite psoriasica ecc). La risonanza magnetica è uno strumento diagnostico di largo impiego nello studio dell’articolazione coxo-femorale, in quanto fornisce un contributo di rilevante interesse nella diagnosi differenziale con altre patologie associate alla presenza di coxalgia. Nella coxartrosi la risonanza magnetica risulta particolarmente sensibile nell’evidenziare la riduzione della rima articolare, la sclerosi subcondrale, gli osteofiti, le cisti e le precoci alterazioni a livello della membrana sinoviale e della cartilagine articolare, in particolare dopo somministrazione endovenosa di mezzo di contrasto paramagnetico (gadolinio) (Jaremko JL, et al. J Rheumatol. 2019). L’utilizzo di sequenze e di piani di sezione appropriati permette, infatti, la precoce individuazione dell’assottigliamento della cartilagine articolare, dell’ispessimento della trabecolatura ossea a livello acetabolare e della testa femorale, delle piccole lesioni cistiche subcondrali e degli osteofiti (Stelzeneder D, et al. Osteoarthritis Cartilage. 2012). La risonanza magnetica consente, inoltre di identificare le alterazioni di segnale riferibili alla presenza di un’osteonecrosi della testa femorale che può essere associata o precedere la degenerazione artrosica
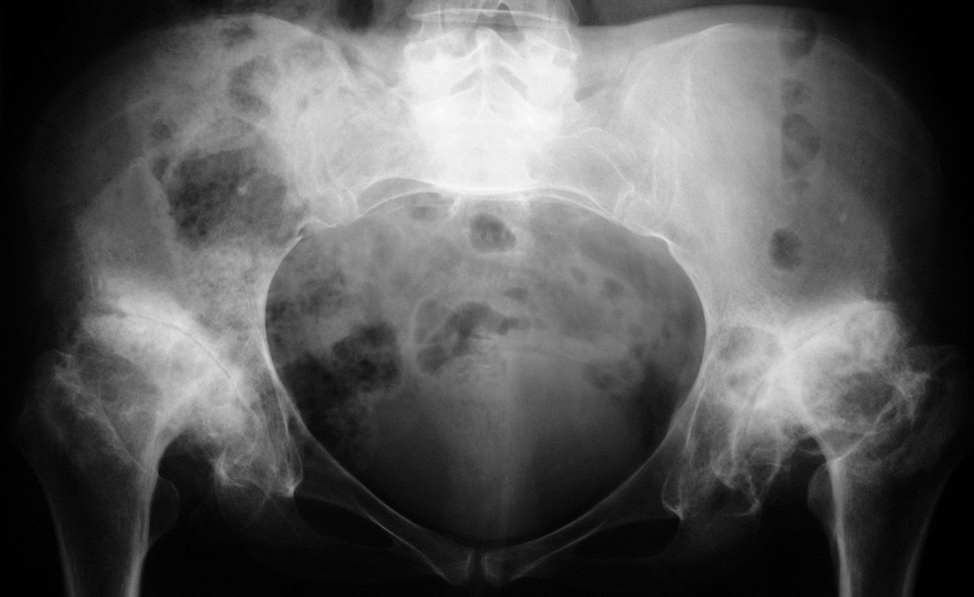
Figura 17: Grave coxartrosi bilaterale (IV stadio radiologico secondo la classificazione di Kellgren e Lawrence) su base displasica
ARTROSI DELLA COLONNA CERVICALE
Il reperto più frequentemente evocato a giustificare una sindrome dolorosa cervicale o una cervicobrachialgia è costituito dalla presenza di una “spondilosi cervicale”, una lesione degenerativa che si manifesta radiologicamente già a partire dai 30 anni e che determina sintomi per i quali non esiste uniformità di vedute, dal momento che vi è, nella maggioranza dei casi, notevole dissonanza tra il quadro radiologico e la sintomatologia clinica. I radiogrammi standard in proiezione antero-posteriore e latero-laterale possono fornire una sufficiente indicazione delle condizioni dei corpi vertebrali. La valutazione dinamica in iperflessione ed iperestensione fornirà dettagli supplementari riguardo la mobilizzazione attiva di questo segmento. Le proiezioni oblique sono irrinunciabili e vanno sempre richieste a corredo di quelle antero-posteriori e latero-laterali per documentare eventuali alterazioni di forma e diametro delle strutture foraminali. Le alterazioni degenerative dei dischi intervertebrali (artrosi intervertebrale) del rachide cervicale interessano più del 70% dei pazienti ultrasettantenni. Di solito sono coinvolti più livelli, con predominanza dei metameri cervicali caudali. Il disco intervertebrale maggiormente interessato è il C5-C6, seguito dal C6-C7. Il nucleo polposo degenera e migra attraverso le fissurazioni dell’anulus mentre la riduzione in altezza dello spazio intervertebrale causa una sublussazione delle faccette articolari posteriori e, talvolta, una retrolistesi del corpo. All’interno dei dischi intervertebrali compaiono raccolte radiotrasparenti lineari o circolari, denominati “vacuum phenomena”. Anche l’artrosi uncovertebrale, secondaria all’interessamento delle articolazioni di Luscha, predilige il segmento C5-C6 e C6-C7 (Feydy A, et al. Rheum Dis Clin North Am. 2009). Con il progredire del processo degenerativo a carico del disco le articolazioni unco-vertebrali si avvicinano tra loro, con conseguente reazione produttiva e formazione di osteofiti che, per la loro posizione topografica, tendono ad estendersi verso il forame di coniugazione, riducendone il diametro. Le articolazioni del compartimento posteriore (articolazioni interapofisarie), in particolare a livello dei metameri cervicali medi ed inferiori mostrano lassità, con conseguente ipermobilità (la sublussazione e il disallineamento reciproco delle vertebre viene definito come spondilolistesi degenerativa o pseudospondilolistesi). In alcuni casi di malattia inveterata si osserva un’anchilosi ossea intra-articolare, che può simulare la spondilite anchilosante o l’artrite reumatoide giovanile. L’artrosi interapofisaria può determinare anche stenosi del canale vertebrale, con interessamento del midollo e delle radici nervose. L’ausilio della tomografia assiale computerizzata e della risonanza magnetica hanno reso possibile lo studio dettagliato del midollo spinale, delle strutture ossee e dei diametri del canale vertebrale, dei dischi e delle strutture dei tessuti molli del rachide cervicale. In generale, sebbene entrambe le tecniche siano in grado di fornire preziose informazioni nell’iter clinico di un paziente portatore di una delle varie sindromi cervicali, la risonanza magnetica è da preferire per lo studio della degenerazione discale, in quanto consente di evidenziare le caratteristiche modificazioni dell’intensità del segnale del disco intervertebrale ed il concomitante interessamento dei corpi vertebrali adiacenti. Essa consente, inoltre, di individuare precocemente le fissurazioni dell’anello fibroso e le migrazioni del nucleo, così come la stenosi del canale vertebrale. La risonanza magnetica si è dimostrata anche più sensibile della TC nello studio delle alterazioni midollari e delle radici nervose.
Sul piano clinico la cervicoartrosi può essere classificata in tre differenti tipologie (Feydy A, et al. Rheum Dis Clin North Am. 2009):
- Cervicoartrosi asintomatica, caratterizzata dai soli reperti radiografici, con eventuale presenza di moderata e non dolorosa limitazione dei movimenti attivi di rotazione ed inclinazione laterale del capo.
- Cervicoartrosi sintomatica semplice, dominata da dolore, cupo, sordo e terebrante, che manifesta esacerbazioni improvvise di breve durata (3-4 giorni), e si irradia fino ai trapezi e/o meno frequentemente al deltoide, alla regione occipitale ed alla zona sovraorbitaria. E’ frequente la contrattura della muscolatura paravertebrale e la limitazione funzionale (torcicollo classico). In taluni casi, è possibile registrare un ricco corteo sintomatologico (cefalea nucale, senso di vertigine, nausea, disestesie/parestesie del volto) di non sempre facile interpretazione.
Cervicoartrosi complicata. A seconda del livello rachideo interessato si realizzano quadri diversi: a) cervico-cefalee con sindromi radicolari superiori C1-C2; b) cervicobrachialgie nelle sindromi C3-T1. La sintomatologia varia in rapporto alle cause eziopatogenetiche. Nelle ernie il dolore è intenso e si associa a rigidità cervicale e ad atteggiamenti antalgici (l’arto superiore é atteggiato in abduzione per detendere la radice compressa). Nelle unco-discoartrosi la rigidità cervicale è di grado inferiore. Nelle mielo-radicolopatie si associano impaccio delle mani, della deambulazione, parestesie agli arti, disturbi sfinterici. Il dolore può peggiorare con la flessione del collo per stiramento delle radici compresse. Nelle radicolopatie a carico della porzione superiore del rachide cervicale (in particolare della C2) il dolore si manifesta principalmente in sede nucale. La radicolopatia C3 provoca dolore e parestesie alla base del collo ed in regione sovra-claveare. La radicolopatia C4 ha una distribuzione della sensibilità a “spallina” con ipovalidità dei muscoli extrarotatori della spalla. La radicolopatia C5 si estende dalla regione deltoidea sino al gomito con deficit sensitivo lungo il lato esterno del braccio. La radicolopatia C6 si manifesta con dolore irradiato alla spalla e all’arto superiore. Concomita un deficit sensitivo a carico del lato esterno dell’avambraccio e del pollice. La radicolopatia C7 provoca dolore alla faccia posteriore dell’arto superiore, dalla spalla al polso con un deficit sensitivo a livello della faccia posteriore dell’avambraccio, dell’indice e del medio. La radicolopatia C8 si associa a dolore al lato interno del braccio e dell’avambraccio con deficit sensitivo dell’anulare e del mignolo. La radicolopatia T1 irradia il dolore al lato interno del braccio fino al terzo prossimale dell’avambraccio con deficit sensitivo che interessa il lato ulnare dell’avambraccio. Per lo studio delle radicolopatie (soprattutto quelle C5-C6, C6-C7 e C7-C8), la cui causa è più frequentemente riconducibile ad un “ernia molle”, talora espulsa, la risonanza magnetica è l’indagine da preferire, in considerazione del miglior contrasto naturale rispetto alla tomografia computerizzata. Le immagini in sezione sagittale mostrano chiaramente l’estensione dell’ernia e dei suoi rapporti con le strutture midollari. L’interessamento artrosico delle articolazioni unco-vertebrali (uncoartrosi) mostra un’evoluzione più lenta rispetto alle radicolopatie indotte da “ernia molle”, con parestesie e ipoestesie che prevalgono sul dolore. L’estensione e la rotazione del capo peggiorano il dolore radicolare. Si possono associare acufeni, vertigini, oscuramento transitorio della vista, cefalea, che configurano la sindrome di Neri-Barrè-Lieu (o sindrome del simpatico cervicale posteriore), per verosimile compressione dell’arteria vertebrale con i movimenti del collo da parte degli osteofiti. Altre volte tale sintomatologia è più grave per l’associarsi di una vera insufficienza vertebro-basilare con “drop-attack”, cioè perdita, in seguito ai movimenti di iperestensione della testa, del controllo degli arti inferiori senza perdita di coscienza. In pazienti con canale midollare stretto (così definito dalla tomografia computerizzata o dalla risonanza magnetica quando il diametro antero-posteriore è inferiore a 13-14 mm) le lesioni artrosiche possono determinare quadri, anche gravi, di mieloradicolopatie.
ARTROSI DELLA COLONNA DORSALE
L’artrosi della colonna dorsale è anch’essa frequente sul piano radiologico, ma i sintomi correlati sono meno facilmente interpretabili e clinicamente meno rilevanti rispetto a quelli dell’artrosi del rachide cervicale e lombare. Solo raramente l’artrosi dorsale è responsabile di una sintomatologia dolorosa clinicamente rilevante che necessita di accurata diagnosi differenziale con altre condizioni, quali le fratture vertebrali da osteoporosi, le metastasi ossee, le neoplasie polmonari e, nei soggetti giovani, le spondiliti e le spondilodisciti. Nella colonna dorsale le alterazioni degenerative si manifestano principalmente a livello toracico medio ed inferiore. Oltre all’artrosi intervertebrale ed interapofisaria è possibile riscontrare, in questo distretto, l’artrosi costo-vertebrale. Le vertebre e le coste si articolano a due livelli: corpo vertebrale con la testa della costa da un lato ed apofisi trasverse con collo e tubercolo costale (articolazioni costo-trasversarie) dall’altro. Le alterazioni degenerative predominano a livello delle articolazioni della D11 e D12. La dimostrazione radiologica di questa localizzazione è difficile, a causa del sovrapporsi delle opacità dei corpi vertebrali e delle coste, tuttavia, talvolta si osservano dei ponti ossei tra la vertebra e la costa, associati ad ispessimento corticale ed iperostosi dell’estremo costale posteriore, con aspetti “simil pagetoidi”.
ARTROSI DELLA COLONNA LOMBARE
L’artrosi della colonna lombare è molto frequente, ed il dolore lombare, che da un punto di vista epidemiologico colpisce l’80% delle persone, almeno una volta nella vita, va differenziato in dolore di origine vertebrale o extravertebrale. Il dolore vertebrale è nella stragrande maggioranza dei casi (circa il 90%) di tipo meccanico per sofferenza locale, provocata da stenosi lombare, dalla presenza di alterazioni vertebrali congenite (sacralizzazione della quinta lombare, lombarizzazione delle vertebre sacrali, asimmetria delle faccette, schisi dell’arco posteriore, spondilolisi-spondilolistesi) o acquisite. Le alterazioni anatomo-patologiche che interessano tanto il nucleo polposo che l’anello fibroso si manifestano radiologicamente come riduzione dello spazio discale, la sclerosi ossea reattiva delle limitanti somatiche superiori ed inferiori e l’osteofitosi marginale (Figura 18) (Goode AP, et al. Arthritis Care Res (Hoboken). 2012). La presenza di varianti morfologiche congenite della giunzione lombo sacrale è frequente e possono essere evidenziate articolazioni neoformate tra le apofisi trasverse iperplasiche della vertebra interessata e le ali del sacro (più raramente dell’ileo), uni o bilateralmente. I processi artrosici di queste articolazioni possono determinare un restringimento dello spazio articolare, con formazione di sclerosi e di osteofiti. Le cause acquisite possono essere di origine muscolare (stiramento o strappi) o discale (degenerazione o ernia del nucleo polposo). Va notato che una vera ernia del disco è rara, mentre è assai più comune la degenerazione discale con conseguente protrusione del disco: l’anello fibroso si fissura, il nucleo migra facendosi strada fra le fissurazioni, quando viene a contatto con le parti più esterne dell’anello fibroso e/o il ligamento longitudinale posteriore, ricchi di nocicettori, dà luogo alla comparsa del dolore. Il passo successivo di questa migrazione del nucleo è l’ernia. I termini di “protrusione” e di “ernia” dovrebbero, pertanto evocare due entità distinte dal punto di vista anatomo-patologico: dà una parte il debordare di un disco degenerato rispetto alle limitanti somatiche (la protrusione), dall’altra l’estrusione del nucleo polposo del disco attraverso un’interruzione dell’anulus (l’ernia). Nessuna delle tecniche di imaging non invasive (tomografia computerizzata o risonanza magnetica) consente un’analisi qualitativa del materiale discale sporgente e in particolare se si tratti di nucleo polposo o meno. L’attribuzione dei due termini è legata, pertanto, a fattori morfologici e quantitativi. Con protrusione si deve intendere il debordare del disco di modesta entità e ad ampio raggio, mentre con ernia si deve intendere il debordare focale e d’entità importante. La sintomatologia del dolore d’origine discale è ad esordio improvviso, acuto, connesso con sforzi o attività lavorative o, talora, con un movimento brusco in flessione (lumbago o colpo della strega). Al dolore si associa uno spasmo localizzato della muscolatura lombare ed impotenza funzionale. La regressione della sintomatologia avviene spontaneamente in un arco temporale compreso fra un minimo di una settimana ed un massimo di due mesi. L’ernia può complicarsi con la comparsa di segni e/o sintomi di compromissione neurologica da conflitto disco-radicolare che provoca intenso dolore a carattere radicolare agli arti inferiori, spesso associato a parestesie. In questi casi è necessario escludere l’esistenza di una stenosi del canale vertebrale lombare. La sintomatologia relativa è quella della “claudicatio intermittens” neurologica: presenza di turbe sensitive (parestesie più o meno dolorose a livello di natiche, cosce e gambe che non hanno una distribuzione radicolare precisa) e motorie (sensazione di debolezza che costringe ad arrestarsi). La sintomatologia insorge con la marcia, dopo aver percorso una certa distanza, o con la posizione eretta prolungata e si allevia solo in posizione seduta o a letto. La claudicatio neurologica va differenziata da quella vascolare, dovuta ad arteriopatia; in questo caso è presente un deficit di pulsatilità delle arterie degli arti inferiori ed i dolori scompaiono non appena si arresta la marcia.
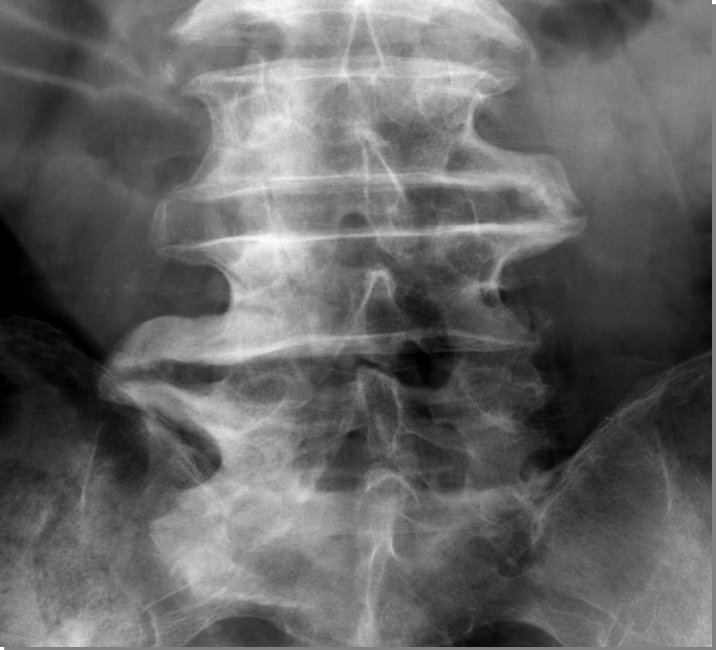
Figura 18: Artrosi della colonna lombare. Nel radiogramma in proiezione antero-posteriore si evidenzia restringimento dello spazio discale nel tratto distale e marcata osteofitosi marginale del rachide lombare
Metodi di valutazione della progressione radiologica in radiologia convenzionale
Analogamente all’artrite reumatoide ed alle spondilo-entesoartriti, anche nell’artrosi sono stati proposti diversi metodi di scoring radiologici, volti, non solo a valutare l’entità del danno osteo-articolare, ma anche per lo studio della progressione radiologica nel tempo e la risposta ai farmaci “disease modifying” (Zhang W, et al. Ann Rheum Dis. 2005). Esistono metodi di scoring globali per la lettura di un largo numero di radiografie e per studi epidemiologici di prevalenza dell’artrosi evidenziabile radiologicamente e metodi di “scoring” dettagliati, che punteggiano le singole lesioni, per identificare dei subset di pazienti e per valutare la progressione radiologica dell’artrosi nei vari distretti di interesse, in particolare la mano, il ginocchio e l’anca (Salaffi F, et al. Aging Clin Exp Res. 2003).
METODI DI VALUTAZIONE DELLE PROGRESSIONE RADIOLOGICA DELLA MANO
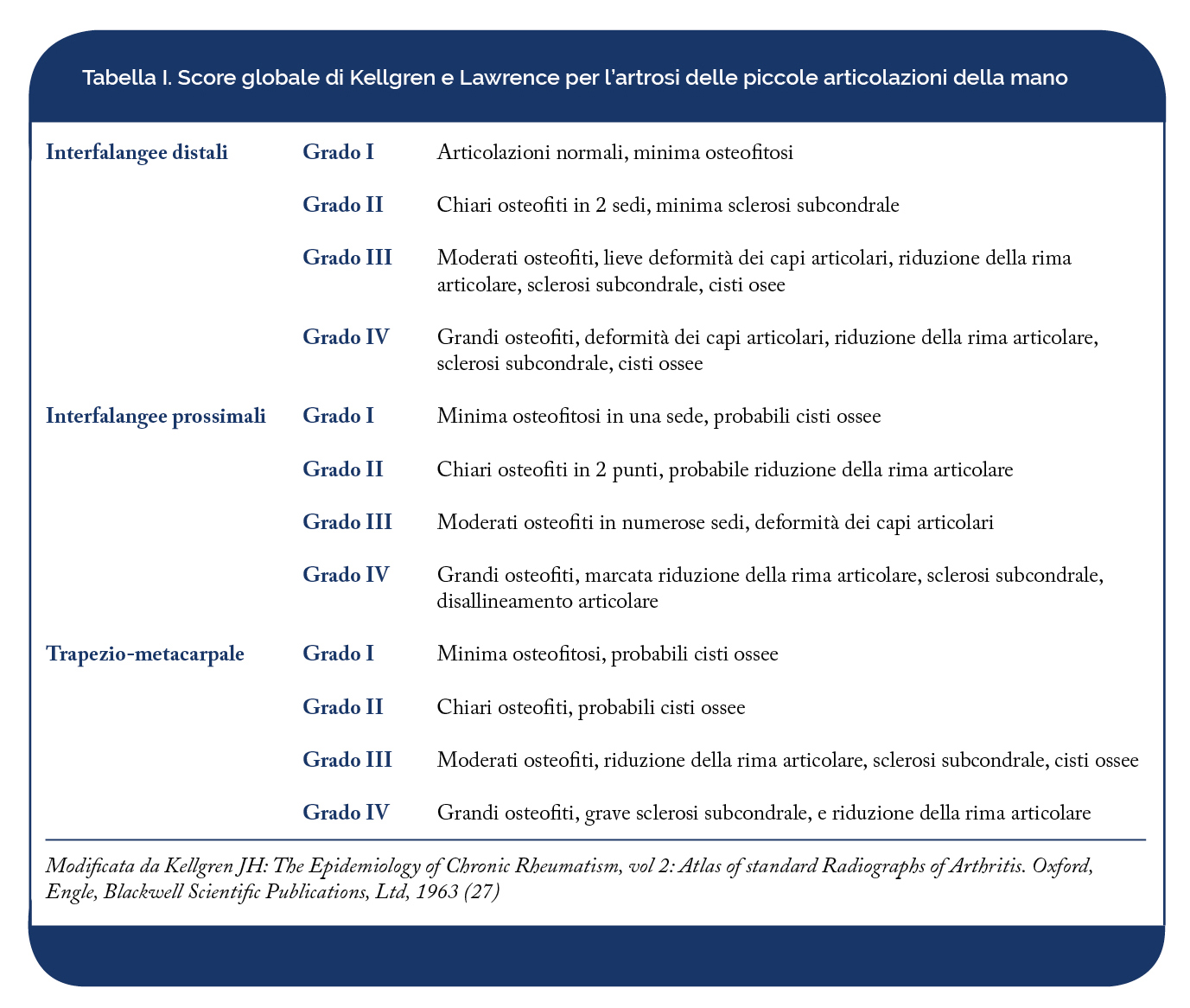
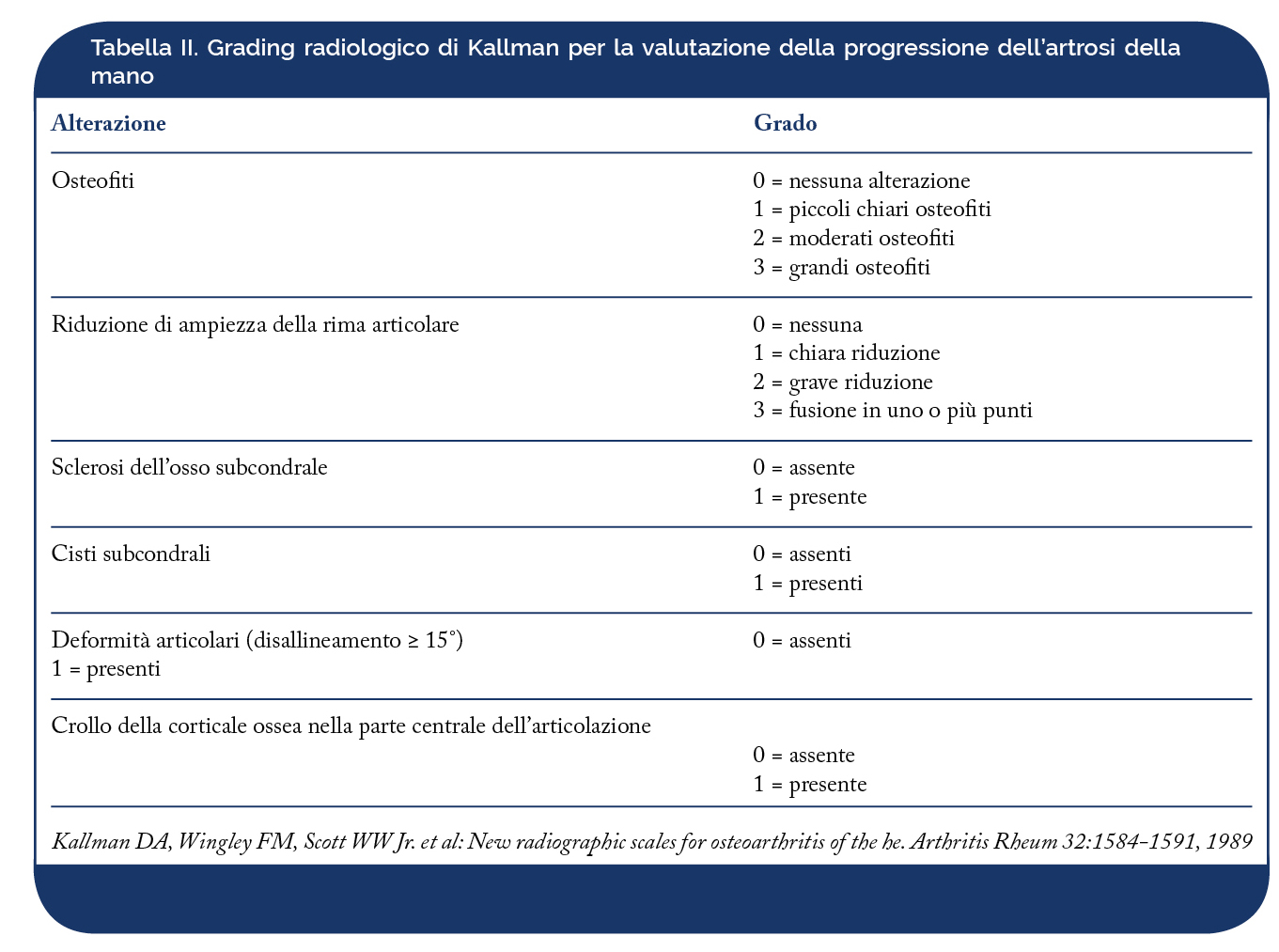
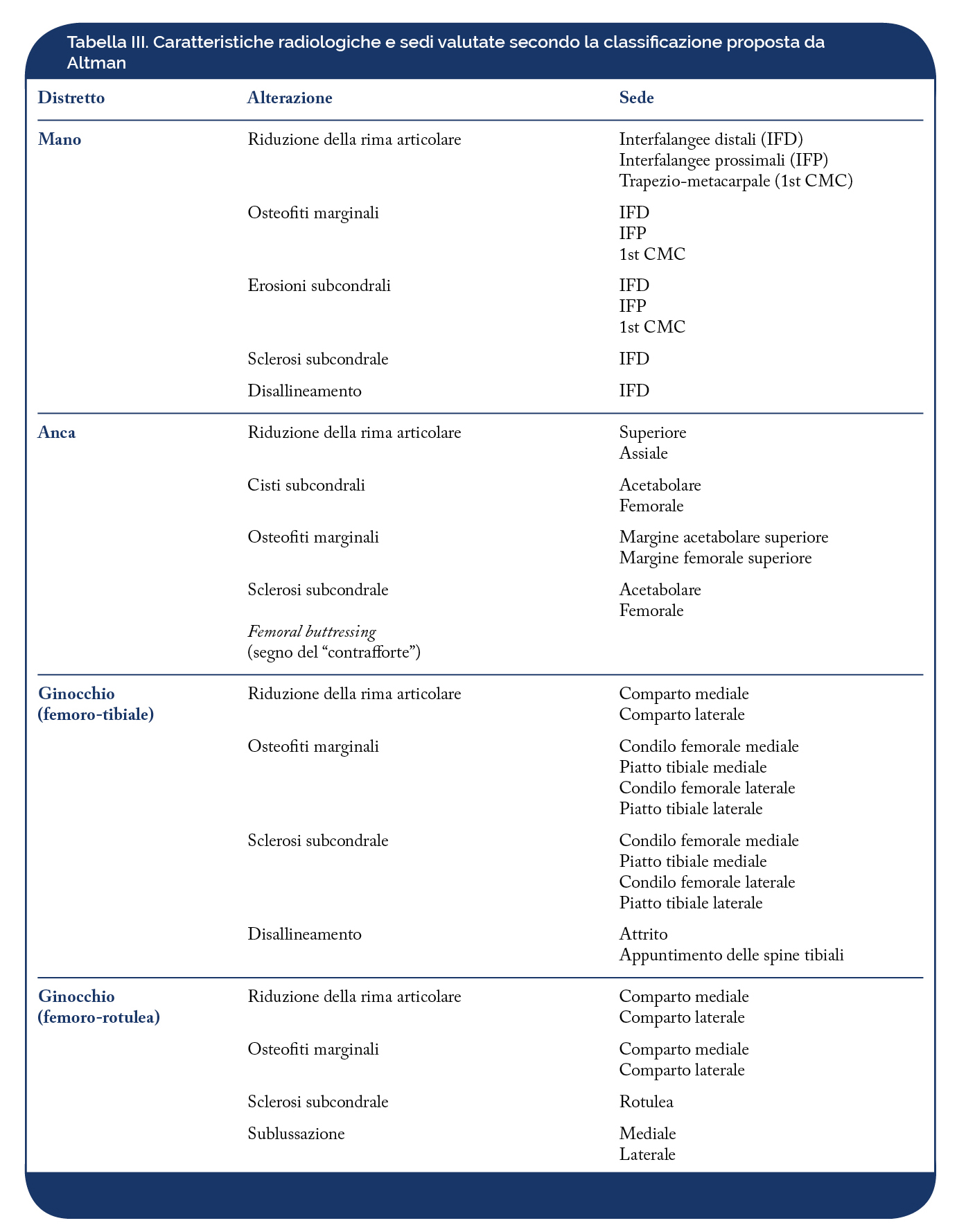
Il primo metodo proposto per lo studio dell’artrosi della mano è stato quello di Kellgren e Lawrence nel 1963. Si tratta di uno score globale, con un grading da I a IV, in cui le lesioni tipiche in corso di artrosi, quali gli osteofiti, la riduzione della rima articolare, la sclerosi e le cisti subcondrali, vengono valutate globalmente a livello delle articolazioni IFD, IFP, la prima articolazione carpo-metacarpale (Tabella I). Tale metodo radiologico si basa sulla presenza dell’osteofita, che è considerato il segno patognomonico, mentre le altre lesioni sono aspecifiche, a meno che non siano presenti in concomitanza con gli osteofiti. Nel 1989 Kallman ha proposto uno metodo che punteggiava secondo uno scoring di gravità da 0 a 3 gli osteofiti e la riduzione della rima articolare, mentre per le altre lesioni quali la sclerosi subcondrale, il collasso centrale, le cisti subcondrali e le deformità articolari viene utilizzato uno score dicotomico: assente o presente (Tabella II). Le articolazioni valutate sono le 5 IFD, le 4 IFP, la prima carpo-metacarpale (in cui la riduzione della rima articolare ha uno score dicotomico: assente o presente) e la trapezio-scafoidea (in cui viene valutata solo la riduzione della rima articolare e non gli osteofiti). Tale metodo è risultato affidabile e riproducibile, con una buona concordanza inter-osservatore, tuttavia i radiogrammi standard pubblicati sono risultati difficili da leggere. Secondo la teoria di Kallman la storia naturale dell’artrosi prevede tre fasi: precoce, intermedia e finale. I dubbi osteofiti (non considerati diagnostici da Kellgren) e la parziale riduzione della rima articolare, valutati insieme o separatamente rappresentano importanti predittori di progressione di malattia. Le fasi intermedia e finale corrispondono agli stadi 3 e 4 del metodo di Kellgren. Nel 1987 Altman ha proposto uno scoring che punteggiava separatamente le singole lesioni evidenziabili radiologicamente, quali gli osteofiti marginali, la riduzione della rima articolare, le erosioni subcondrali, la sclerosi subcondrale e la sublussazione o disallineamento, secondo un punteggio compreso tra 0 e 3 (Tabelle III e IV). Le articolazioni valutate sono le IFD, le IFP, la IF del 1° dito e la trapezio-metacarpale. La sclerosi subcondrale e la sublussazione vengono valutate solo a livello delle IFD. Nel 1995 è stato pubblicato dallo stesso autore un atlante dettagliato per lo studio della progressione radiologica dell’OA nelle sedi più frequentemente colpite: mano (Figura 19), ginocchio ed anca (Salaffi F, et al. Aging Clin Exp Res. 2003).
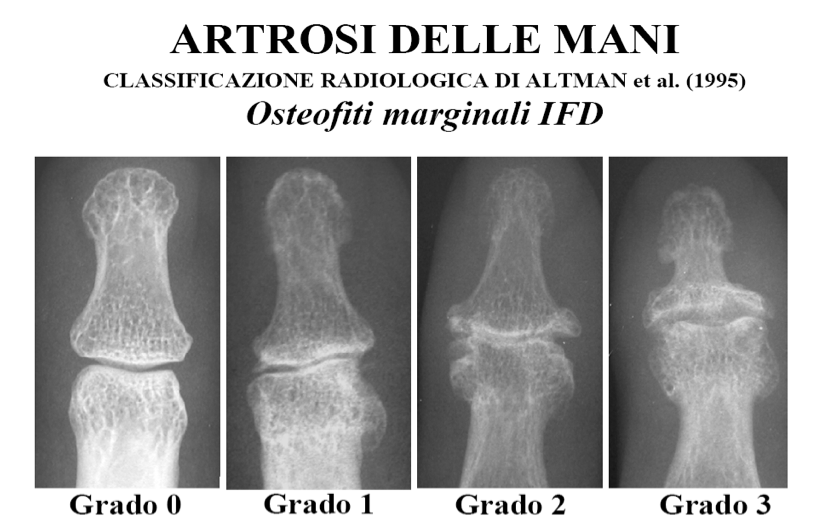
Figura 19. Artrosi delle mani – Classificazione radiologica di Altman. Osteofiti marginali a carico delle articolazioni interfalangee distali.

Nel 1995 Verbruggen propone due tipi di scoring per lo studio della progressione radiologica nel tempo: a) un metodo basato sulla valutazione delle lesioni anatomiche, quali gli osteofiti, le cisti subcondrali e lo spazio articolare a livello delle 8 IFD, delle 8 IFP e delle 8 MCF, secondo un punteggio di ± 0.5 e ± 0.1; b) l’altro metodo basato sul punteggio delle fasi anatomiche: N= normale, S= stazionario, J= completa perdita dello spazio articolare, E= cisti subcondrali, con erosioni del piatto subcondrale e pseudoallargamento dello spazio articolare, R= rimodellamento osseo. A ciascuna di queste fasi viene assegnato uno score arbitrario per lo studio della progressione radiologica dell’artrosi (Figura 20). Secondo lo stesso autore il punteggio delle singole lesioni radiologiche è piuttosto laborioso ed il riconoscimento delle diverse fasi anatomiche e l’assegnazione di score a queste fasi semplifica la procedura e conduce alle stesse conclusioni. Nel 2000 Kessler, riferendosi all’atlante di Altman, propose un semplice score dicotomico, in cui un’articolazione è o non è coinvolta dal processo artrosico. In questo metodo la riduzione della rima articolare, essendo un segno indiretto di perdita della cartilagine articolare, rappresenta il parametro discriminante, mentre le altre lesioni vengono considerate solo in associazione alla riduzione della rima articolare. Tale metodo risulta particolarmente utile per studi epidemiologici di prevalenza e per calcolare il numero di articolazioni interessate dal processo artrosico (Salaffi F, et al. Aging Clin Exp Res. 2003).
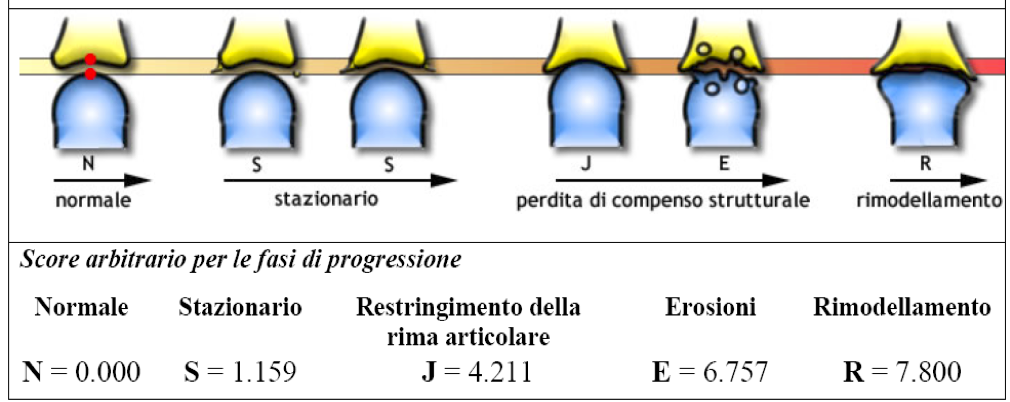
Figura 20. Rappresentazione schematica delle fasi di progressione del danno strutturale in corso di artrosi delle articolazioni interfalangee
METODI DI VALUTAZIONE DELLA PROGRESSIONE RADIOLOGICA DEL GINOCCHIO
Il primo metodo proposto per lo studio della gonartrosi è stato quello di Kellgren e Lawrence. Si tratta di uno score globale a quattro livelli di gravità (da 0 a 4), con il quale vengono valutate le alterazioni radiologiche tipiche in corso di gonartrosi, quali gli osteofiti marginali, la riduzione della rima articolare, la sclerosi subcondrale e le deformità articolari (Tabella V) (Figura 21) (Emrani PS, et al. Osteoarthritis Cartilage. 2008). L’atlante di riferimento proposto da Altman nel 1995 prevedeva, oltre alla valutazione semiquantitativa del danno radiologico a carico della mano, anche quella del ginocchio e dell’anca, secondo un grading da 0 a 3 delle singole alterazioni evidenziabili radiologicamente (Tabelle III e IV). Per la gonartrosi vengono punteggiati: la riduzione della rima (a livello del comparto mediale e laterale), gli osteofiti marginali (sui condili femorali mediale e laterale e sui piatti tibiale mediale e laterale), la sclerosi subcondrale (a livello dei condili femorali mediale e laterale e dei piatti tibiali mediale e laterale) e il malallineamento per l’articolazione femoro-tibiale e gli osteofiti marginali (a livello del comparto mediale e laterale), la riduzione della rima articolare (comparto mediale e laterale), la sclerosi subcondrale (sul versante patellare) e la sublussazione (laterale e mediale) per l’articolazione femoro-rotulea. Nel corso degli anni sono stati proposti altri metodi di scoring qualitativi o semiquantitativi per lo studio della progressione radiologica, in cui viene punteggiata la riduzione della rima articolare, secondo 4 livelli di gravità, o gli osteofiti mediante scala analogica visiva a 4 livelli e score globali per riduzione della rima articolare, appuntimento delle spine tibiali e sclerosi secondo un punteggio da 0 a 4 (Tabella V) (Salaffi F, et al. Aging Clin Exp Res. 2003).
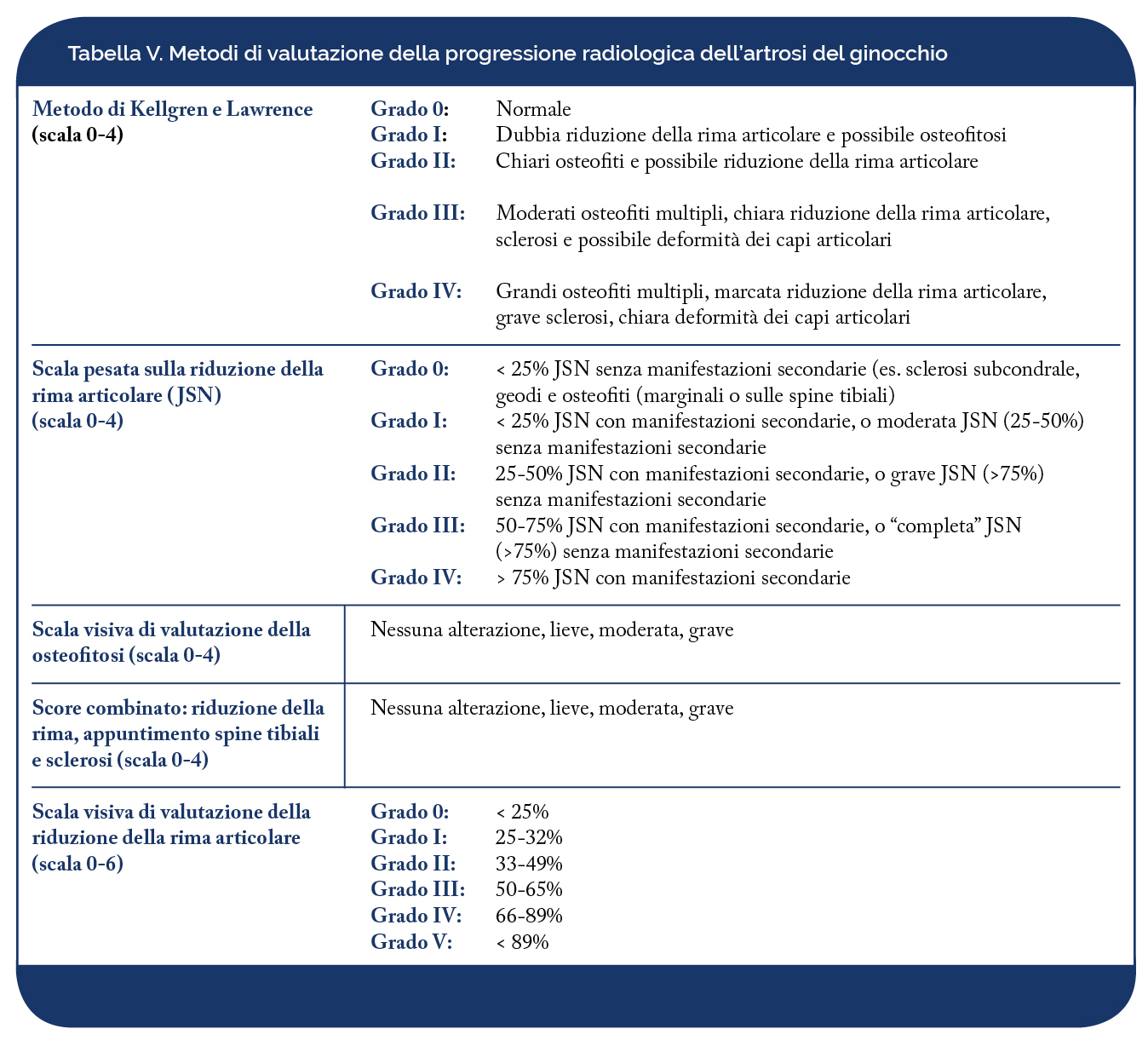
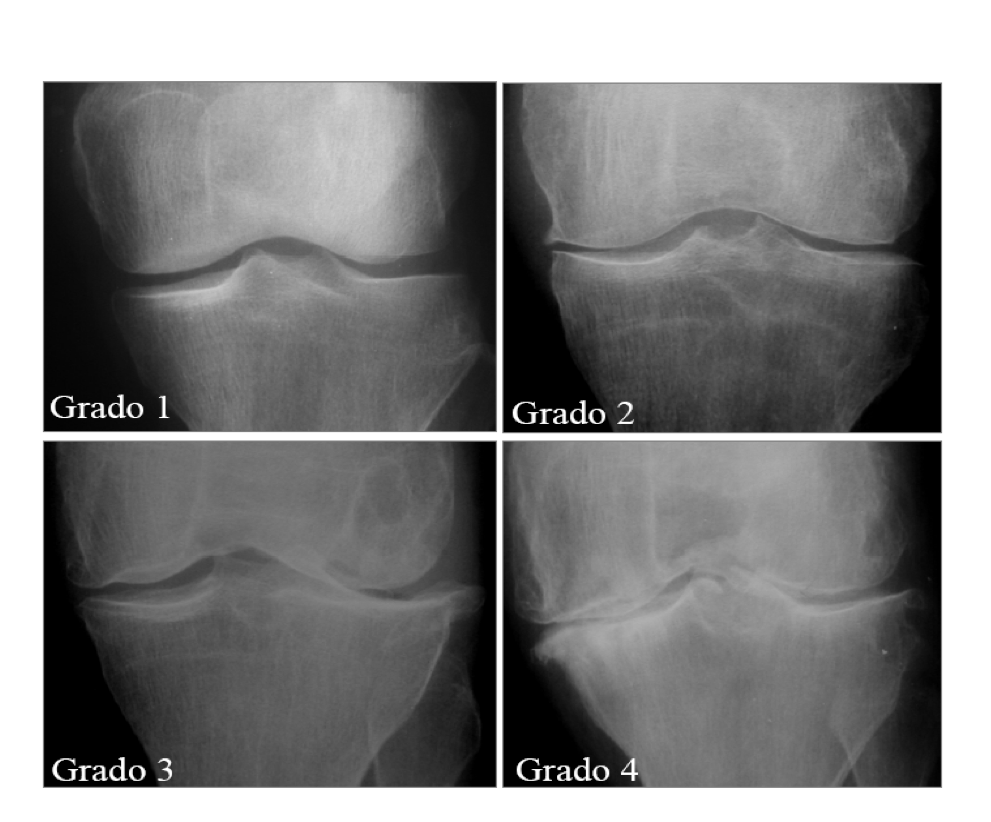
Figura 21. Artrosi delle ginocchia – Classificazione radiologica secondo Kellgren & Lawrence.
METODI DI VALUTAZIONE DELLA PROGRESSIONE RADIOLOGICA DELL’ANCA
Come per la mano ed il ginocchio, Kellgren e Lawrence proposero uno metodo radiologico che valuta globalmente, secondo uno score compreso fra I e IV, le alterazioni radiologiche tipiche in corso di coxartrosi, quali gli osteofiti marginali, la riduzione della rima articolare, la sclerosi subcondrale, le cisti e le deformità della testa femorale e dell’acetabolo (Tabella VI) (Figura 22). Nel 1990, analogamente a Kellgren, Croft et al proposero un metodo semiquantitativo, che prevedeva una valutazione composita delle alterazioni radiologiche in corso di artrosi, secondo un grading compreso fra 0 e 5: grado 0 = normale; grado 1 = solo osteofitosi; grado 2 = solo riduzione dello spazio articolare; grado 3 = due delle seguenti alterazioni: osteofitosi, riduzione della rima articolare, sclerosi subcondrale e formazione di cisti; grado 4 = tre delle seguenti alterazioni: osteofitosi, riduzione della rima articolare, sclerosi subcondrale e formazione di cisti; grado 5 = come il grado 4, ma con deformità della testa femorale. È stato, inoltre, proposto uno score radiologico che punteggia singolarmente le alterazioni radiologiche secondo una scala di gravità compresa fra 0 e 3 per la riduzione della rima articolare e gli osteofiti e fra 0 e 1 (presente/assente) per la sclerosi, le erosioni o le cisti e le deformità articolari. Nel 1995, Altman ha proposto un atlante di riferimento ed uno scoring radiologico per la valutazione semiquantitativa del danno radiologico a carico dell’anca. Tale scoring radiologico prevede la valutazione delle singole alterazioni radiologiche, assegnando un punteggio tra 0 e 3 per gli osteofiti marginali, la riduzione della rima articolare, le cisti subcondrali, la sclerosi subcondrale e l’ispessimento a “contrafforte”, a livello del margine mediale del collo femorale (Salaffi F, et al. Aging Clin Exp Res. 2003).

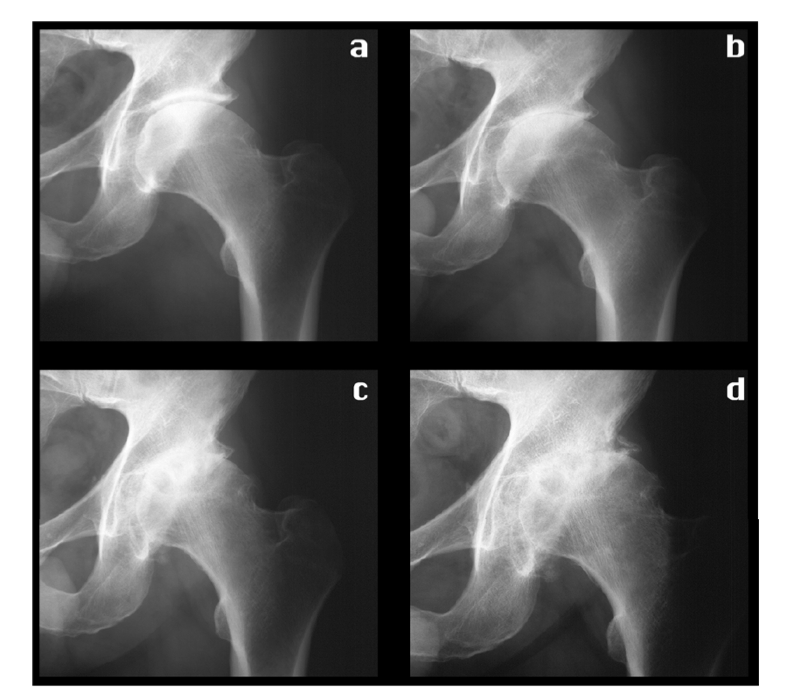
Figura 22. Artrosi delle anche – Classificazione radiologica secondo Kellgren & Lawrence
Aspetti metodologici correlati alla valutazione della progressione radiologica in radiologia convenzionale
Come per l’artrite reumatoide nello studio dell’artrosi della mano viene comunemente utilizzata la sola proiezione postero-anteriore, in quanto le altre proiezioni (come la Norgaard e la Brewerton) aumentano la visibilità, in particolare a livello delle IFP, oltre che delle MCF, ma ciò comporta parallelamente una penalizzazione in termini di riproducibilità (Hellio Le Graverand MP, et al. Semin Arthritis Rheum. 2013). Per quanto, invece, attiene lo studio della progressione radiologica delle articolazioni sotto carico, in particolare del ginocchio e dell’anca, sia in studi epidemiologici che nei trial clinici, il miglior criterio è rappresentato dalla valutazione del danno cartilagineo, espresso dalla misura dello spazio articolare medio. Tuttavia, per ottenere misure affidabili, utili allo studio della progressione radiologica, con radiologia tradizionale, è indispensabile attenersi a procedure standardizzate, in quanto le fonti di variabilità possono essere molteplici (Tabelle VII e VIII). La procedura radiologica (inclinazione del fascio di raggi X), il posizionamento del paziente (radiogramma sotto carico o in posizione supina, appoggio mono o bipodalico, rotazione dei piedi, ginocchia estese o in semiflessione), la sede di misurazione, il metodi di misurazione (automatici o non), il training del lettore o il numero dei lettori sono solo alcune delle possibili fonti di errore. Di particolare importanza per garantire le caratteristiche di affidabilità risultano essere la standardizzazione della tecnica utilizzata ed il posizionamento del paziente. La distanza fuoco-film dovrebbe essere di 100-110 cm, con il fascio di raggi X parallelo al suolo, perpendicolare alla pellicola radiografica e allineato con il centro dell’articolazione in studio. A questo scopo, sono stati sviluppati diversi protocolli radiologici standardizzati, alcuni dei quali si avvalgono dell’ausilio della fluoroscopica o di guide di posizionamento, per ottenere il corretto allineamento radio-anatomico delle strutture in esame (Salaffi F, et al. Aging Clin Exp Res. 2003).


Per la valutazione dell’articolazione femoro-tibiale sono state proposte diverse tecniche (Figura 23 a-b-c-d-e) (Piperno M, et al. Osteoarthritis Cartilage. 1998):
- proiezione antero-posteriore in estensione: sotto carico, con le ginocchia estese e la parte posteriore del ginocchio a contatto con il porta pellicole verticale (Figura 23a). Per molti anni è stata considerata la proiezione standard, ed è tuttora utilizzata per identificare le lesioni ossee elementari in corso di gonartrosi (osteofiti, sclerosi subcondrale). I principali limiti di questa proiezione, riguardano la scarsa riproducibilità nelle misure dello spessore della cartilagine articolare, convenzionalmente calcolato come spazio articolare a livello del comparto femoro-tibiale mediale. Questo limite è legato alla variabilità del posizionamento del paziente in misure seriali (variabilità nei gradi di estensione a causa del dolore, mancata standardizzazione dell’ allineamento del fascio di raggi X e del piatto tibiale mediale, variabilità della distanza tra il ginocchio e la cassetta porta pellicola;
- proiezione antero-posteriore in semiflessione: con le ginocchia in leggera flessione (7-10°), il fascio di raggi X parallelo alle superfici articolari o inclinato di 5° verso il basso e le rime tibiali anteriore e posteriore sovrapposte, posizionate sotto guida fluoroscopica. I piedi vengono ruotati finchè le spine tibiali non risultano centrate al di sotto della gola intercondiloidea (Figura 23b);
- proiezione postero-anteriore (tunnel view): con le ginocchia in leggera flessione (20°) ed il fascio di raggi X inclinato verso il basso di 10°. Entrambe le ginocchia sono a contatto con la cassetta radiografica e coplanari con le anche, le rotule e la punta delle prime dita. Non si utilizza la guida fluoroscopica. I calcagni vengono fissati ed i piedi ruotati esternamente di 10° (Figura 23c).
- proiezione postero-anteriore di Lyon-Schuss: con le ginocchia in leggera flessione (20-35°), le cosce e rotule a contatto con il porta pellicole verticale, coplanari con il margine anteriore dell’anca e con le punte degli alluci. Il fascio di raggi X ha una angolazione variabile in funzione dell’allineamento con il piatto tibiale mediale. I piedi vengono ruotati internamente o esternamente, in modo che, sotto guida fluoroscopica, le spine tibiali risultino centrate al di sotto della gola intercondiloidea (Figura 23d) (Mazzuca SA, et al. Osteoarthritis Cartilage. 2008 – Vignon E, et al. Arthritis Rheum. 2003).
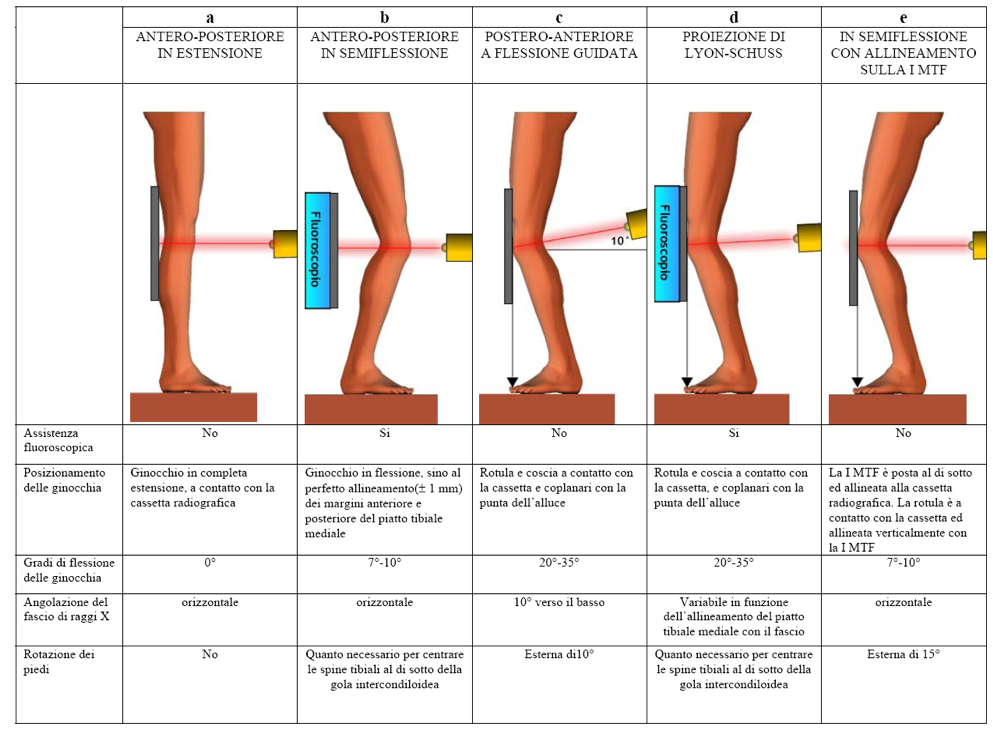
Figura 23: Tecniche per la valutazione dell’articolazione femoro-tibiale in radiologia convenzionale
L’utilizzo di una guida fluoroscopica, presenta sicuramente dei vantaggi in termini di precisione e sensibilità nella evidenziazione e misurazione della rima articolare (Mazzuca SA, et al. Osteoarthritis Cartilage. 2008 – Conrozier T, et al. J Rheumatol. 2004). L’applicazione di questa metodica in studi multicentrici, presenta dei limiti non trascurabili, rappresentati essenzialmente da:
- disponibilità e accessibilità della strumentazione
- training del personale tecnico
- maggior dose di radiazioni assorbita dal paziente
- costo dell’esame (circa 3-4 volte maggiore rispetto alle tecniche senza guida fluoroscopica)
E’ stato proposto e validato un metodo radiologico basato sul posizionamento del paziente in ortostatismo, con le ginocchia in leggera flessione (7°-10°), fino a venire a contatto con il film-cassetta, in proiezione postero-anteriore, con la prima metatarso falangea in linea con il bordo della cassetta. Il raggio incidente è orizzontale ed orientato verso il punto centrale del ginocchio (Figura 23e). Questo metodo ha dimostrato una maggiore precisione nella misurazione dello spazio articolare rispetto alla proiezione convenzionale (antero-posteriore con paziente in piedi) e alla tecnica “tunnel view” (postero-anteriore con le ginocchia in flessione di circa 30°, senza guida fluoroscopica). Tuttavia è fondamentale riuscire ad ottenere l’allineamento del piatto tibiale mediale con il fascio di raggi X, perchè è questo il fattore che, in misura maggiore, compromette la sensibilità delle misurazioni dell’ampiezza della rima articolare (Figura 24) (Vignon E, et al. Arthritis Rheum. 2003).
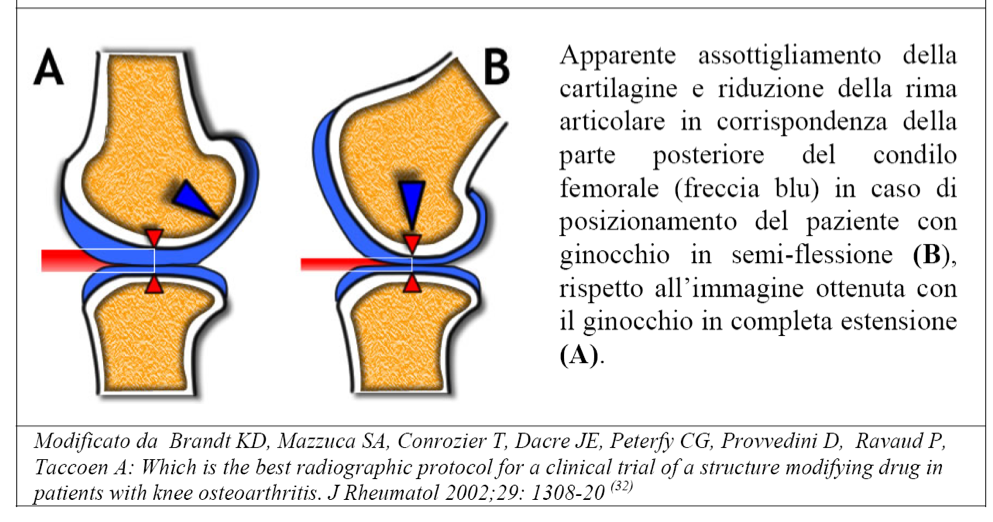
Figura 24. Protocolli radiologici standardizzati per lo studio della gonartrosi: effetti della variazione dell’angolo femoro-tibiale sulla valutazione dell’ampiezza della rima articolare e dello spessore cartilagineo.
La comparazione tra le diverse tecniche, ha dimostrato la maggiore precisione del metodo in semiflessione con allineamento alla I MTF nella misurazione dello score totale della riduzione della rima articolare (somma degli score dei comparti mediale e laterale destro e sinistro), rispetto alla tecnica “tunnel view” e alla proiezione di Lyon-Schuss (Vignon E, et al. Arthritis Rheum. 2003). Attualmente, le linee guida nei trial multicentrici, per lo studio dei farmaci “disease modifying” per l’artrosi, sono a favore dei protocolli che non richiedono la guida fluoroscopica per la standardizzazione del posizionamento del paziente, tuttavia questo non deve prescindere dal training del personale tecnico per raggiungere un alto livello di efficienza tecnica (Tabella IX). Un board di esperti, riunitosi in Francia nel gennaio 2002, ha lasciato aperte molte questioni riguardo al “metodo ideale” da utilizzare per lo studio e il follow-up della variazioni di ampiezza della rima articolare in trial multicentrici sui “disease modifying drugs” per l’artrosi. La conclusione a cui si è giunti è che a tutt’oggi il “metodo ideale” non esiste, e solo studi longitudinali su un maggior numero di pazienti potranno fornire ulteriori informazioni riguardo ai vantaggi della guida fluoroscopica e della standardizzazione del posizionamento radio-anatomico, in particolare dei protocolli in semiflessione o in semiflessione con allineamento alla I MTF. Per l’articolazione femoro-rotulea vengono utilizzate le proiezioni assiali, con il paziente in posizione supina, con i calcagni appoggiati al tavolo radiologico, in modo che le ginocchia siano flesse a 45°. Il fascio di raggi X ha un’angolazione di 30-40° in direzione caudale e perpendicolare al film/cassetta (proiezione di Merchant) (Figura 25).


Figura 25. Studio del compartimento femoro-rotuleo del ginocchio. Proiezione tangenziale.
Per lo studio dell’anca, si raccomanda la proiezione antero-posteriore, con il paziente in posizione supina, i piedi intraruotati di 15° e il fascio di raggi X centrato 2 cm cranialmente alla sinfisi pubica e perpendicolare al tavolo radiologico. La proiezione antero-posteriore sotto carico è raccomandata per lo studio della rima articolare in studi prospettici per la maggiore sensibilità rispetto alla posizione supina (quando la rima articolare è < 2.5 mm). La proiezione antero-posteriore con il paziente supino ed intrarotazione dei piedi di 15° rappresenta lo standard più utilizzato nella pratica clinica, specialmente in pazienti obesi. Analogamente al ginocchio, anche nello studio radiologico dell’anca si riconoscono molteplici fonti di variabilità.
In letteratura esistono diversi metodi quantitativi per misurare l’ampiezza dello spazio articolare, in particolare in studi sulla progressione radiologica in corso di gonartrosi. Lo spazio articolare può essere misurato sia calcolando la distanza a livello del punto centrale dell’articolazione femoro-tibiale o la distanza fra la corticale dell’acetabolo e il contorno osseo della testa femorale per l’anca, o nel punto più ristretto dello spazio articolare, mediante metodi automatici o semi-automatici (analisi computerizzata di immagini digitalizzate) o con metodi non automatici, con l’ausilio di righello, calibro con regolazione micrometrica, lente di ingrandimento graduata, oppure calcolando l’area mediante analisi computerizzata di immagini digitalizzate (Tabella X) (Piperno M, et al. Osteoarthritis Cartilage. 1998).

Fattori di rischio di incidenza e di progressione
Studi epidemiologici ed eziologici sono concordi nel differenziare i fattori di rischio per l’incidenza dell’artrosi e quelli predittivi di progressione radiologica (Riddle DL, et al. Osteoarthritis Cartilage. 2016). Fra i fattori di rischio per l’incidenza figurano: a) il sesso (dopo i 50 anni le donne sono maggiormente esposte all’artrosi, specie quella della mano); b) l’età (la senescenza influisce sul metabolismo cartilagineo, riducendo la resistenza dei condrociti agli stress ossidativi ed alterando le risposte ai fattori di crescita ed alle metalloproteasi); c) l’obesità (una riduzione del peso corporeo determina un calo d’incidenza dell’artrosi dell’anca del 25% ed una perdita di soli 5 kg in soggetti in sovrappeso comporta una diminuzione del 24% degli interventi di protesizzazione del ginocchio) (Niu J et al. Arthritis Rheum. 2009); d) fattori occupazionali (l’uso ripetitivo di determinate articolazioni per lunghi periodi di tempo è associato a specifiche forme d’artrosi) o sportivi (la pratica agonistica è stata ampiamente correlata allo sviluppo di varie forme d’artrosi), e) fattori genetici (alcuni loci mappati sui cromosomi 4 e 16, sul segmento 11q 12-13, sui cromosomi 2, 9, 11, sul cromosoma 6 conferirebbero suscettibilità all’artrosi). E’, inoltre, enfatizzato il ruolo esercitato dai menischi nell’ammortizzare le forze agenti sul ginocchio ed appare, pertanto probabile che le anomalie meniscali o la meniscectomia parziale o totale possano favorire una più precoce e rapida degenerazione della cartilagine articolare. Anche l’osteonecrosi idiopatica del condilo femorale, più frequente nei soggetti d’età medio-avanzata, può condizionare una degenerazione secondaria della sovrastante cartilagine articolare. Fra i fattori di rischio di progressione radiologica figurano l’obesità, quale predittore non radiologico ed il grado iniziale di riduzione della rima articolare, quale maggior predittore di tipo radiologico (Kinds MB, et al. Osteoarthritis Cartilage. 2012). E’ noto che fra i pazienti con gonartrosi sintomatica, coloro che evolvevano più rapidamente verso l’anchilosi articolare, erano quelli che all’inizio presentavano una maggiore riduzione della rima articolare. I dati della letteratura, in merito alla progressione della riduzione della rima articolare nei pazienti con artrosi di ginocchio, hanno riportato un ampio spettro di valori (compresi tra 0.06 e 0.6 mm/anno). Studi di popolazione, come il Baltimore Longitudinal Study of Aging e lo studio Framingham hanno riportato valori intorno a 0.1 mm/anno. Tale valore è stato confermato da un ampio studio a lungo termine su una casistica di pazienti ambulatoriali. Uno studio controllato ha riportato una riduzione media dello spazio articolare a livello del ginocchio pari a 0.31 mm, dopo 3 anni, in pazienti con gonartrosi trattati con placebo rispetto ad una diminuzione media della rima articolare pari allo 0.06 mm evidenziata in pazienti trattati con glucosamina solfato (un farmaco ad azione strutturale). Studi sulla progressione radiologica in pazienti con artrosi dell’anca hanno evidenziato che la velocità di riduzione della rima articolare appare essere lineare nel tempo. E’ stato stabilito un valore di “cut off” di 0.2 mm/anno per suddividere i “lenti progressori” (slow decliners), che avevano una riduzione media della rima articolare £ 0.2 mm/anno, dai “rapidi progressori” (rapid decliners), che mostravano, invece, un rate medio > 0.2 mm/anno. Avendo la riduzione della rima articolare un andamento lineare nel tempo, lo studio della progressione radiologica valutata nei primi 20 mesi di malattia potrebbe fornire al clinico utili informazioni concernenti il follow-up a lungo termine ed individuare il gruppo di pazienti da sottoporre al trattamento con farmaci “structure modifying”. Come per il ginocchio, il valore medio dell’ampiezza dello spazio articolare (calcolato a livello dello spazio supero-laterale, supero-intermedio e supero-mediale) è una misura più sensibile e riproducibile rispetto al valore minimo della rima articolare. Lo sviluppo di nuove strategie per la prevenzione e il trattamento dell’artrosi, richiede una più chiara comprensione dei fattori che sono in grado di influenzare la progressione della malattia. La capacità di quantificare la progressione dell’artrosi è il primo, imprescindibile, passo verso il raggiungimento di questo obiettivo (Karsdal MA, et al. Osteoarthritis Cartilage. 2015).
Conclusione
A tutt’oggi, la radiologia convenzionale, nonostante le più sofisticate tecniche di imaging, come la risonanza magnetica, la tomografia computerizzata, l’ecografia ad alta risoluzione e la scintigrafia per la scarsa invasività, l’ampia disponibilità ed il costo relativamente basso, rappresenta la tecnica più utilizzata, non solo per il riconoscimento delle lesioni elementari in corso di artrosi, ma anche per lo studio della progressione radiologica e riveste un ruolo di primo piano nei processi decisionali in ambito clinico e terapeutico (Braun HJ, et al. Bone. 2012 – Nieminen MT, et al. Osteoarthritis Cartilage. 2019 – Sakellariou G, et al. Ann Rheum Dis. 2017). I risultati dei trial clinici hanno indotto un crescente interesse sulla valutazione del danno osteo-cartilagineo e la sua progressione in corso di artrosi. L’utilizzo di radiografie seriali, è sembrato lo strumento più adatto a tale scopo, a condizione che venga utilizzata una tecnica valida, affidabile e riproducibile. Sarà, pertanto, necessario pervenire alla formulazione di linee guida dettagliate per il posizionamento del paziente, la procedura e la sede di misurazione della rima articolare e il metodo di scoring più sensibile. Queste informazioni potranno essere di supporto al medico nella scelta del trattamento farmacologico o chirurgico nel paziente con artrosi e nel monitoraggio dell’efficacia dell’intervento.
Punti chiave
- A tutt’oggi, nonostante le più moderne tecniche di imaging, la radiologia tradizionale resta una tecnica fondamentale ed irrinunciabile nello studio dell’artrosi, non solo per l’identificazione delle lesioni elementari (riduzione della rima articolare, osteofiti marginali, sclerosi subcondrale e cisti) e dell’entità del danno anatomico, ma anche per la valutazione della progressione radiologica nel tempo e l’indentificazione dei fattori predittivi di progressione radiologica.
- Sono stati proposti e validati numerosi metodi di scoring radiologici semiquantitativi per la valutazione della progressione del danno anatomico nell’artrosi. Essi comprendono scale che prevedono una valutazione globale del danno articolare e scale in cui le singole lesioni evidenziate radiologicamente vengono punteggiate separatamente.
- Sia negli studi epidemiologici che nei trial clinici, allo scopo di ottenere misure affidabili, utili allo studio della progressione radiologica in radiologia convenzionale, è indispensabile attenersi a procedure standardizzate, riconducibili alla tecnica radiologica (inclinazione del fascio di raggi X), al posizionamento del paziente, alla sede di misurazione, al metodo di misurazione, nonché al training del lettore o il numero dei lettori.
Bibliografia
- Nelson AE, Smith MW, Golightly YM, Jordan JM. “Generalized osteoarthritis”: a systematic review. Semin Arthritis Rheum. 2014;43(6):713-20
- Salaffi F, Carotti M, Stancati A, Grassi W. Health-related quality of life in older adults with symptomatic hip and knee osteoarthritis: a comparison with matched healthy controls. Aging Clin Exp Res. 2005;17(4):255-63
- Salaffi F, Carotti M, Grassi W. Health-related quality of life in patients with hip or knee osteoarthritis: comparison of generic and disease-specific instruments. Clin Rheumatol. 2005;24(1):29-37
- Salaffi F, Cavalieri F, Nolli M, Ferraccioli G. Analysis of disability in knee osteoarthritis. Relationship with age and psychological variables but not with radiographic score. J Rheumatol. 1991;18(10):1581-6
- Braun HJ, Gold GE. Diagnosis of osteoarthritis: imaging. Bone. 2012;51(2):278-88
- Nieminen MT, Casula V, Nevalainen MT, Saarakkala S. Osteoarthritis year in review 2018: imaging. Osteoarthritis Cartilage. 2019 Mar;27(3):401-411. doi: 10.1016/j.joca.2018.12.009
- Sakellariou G, Conaghan PG, Zhang W, Bijlsma JWJ, Boyesen P, D’Agostino MA, Doherty M, Fodor D, Kloppenburg M, Miese F, Naredo E, Porcheret M, Iagnocco A. EULAR recommendations for the use of imaging in the clinical management of peripheral joint osteoarthritis. Ann Rheum Dis. 2017 Sep;76(9):1484-1494
- Mathiessen A, Cimmino MA, Hammer HB, Haugen IK, Iagnocco A, Conaghan PG. Imaging of osteoarthritis (OA): What is new? Best Pract Res Clin Rheumatol. 2016 ;30(4):653-669
- Boesen M, Ellegaard K, Henriksen M, Gudbergsen H, Hansen P, Bliddal H, Bartels EM, Riis RG. Osteoarthritis year in review 2016: imaging. Osteoarthritis Cartilage. 2017 Feb;25(2):216-226. doi: 10.1016/j.joca.2016.12.009
- Guermazi A, Roemer FW, Crema MD, Englund M, Hayashi D. Imaging of non-osteochondral tissues in osteoarthritis. Osteoarthritis Cartilage. 2014;22(10):1590-605)
- Hayashi D, Roemer FW, Guermazi A. Imaging for osteoarthritis. Ann Phys Rehabil Med. 2016;59(3):161-169)
- Hayashi D, Roemer FW, Guermazi A. Osteoarthritis year 2011 in review: imaging in OA–a radiologists’ perspective. Osteoarthritis Cartilage. 2012;20(3):207-14).
- Addimanda O, Cavallari C, Pignotti E, Pulsatelli L, Mancarella L, Ramonda R, Fioravanti A, Meliconi R. Radiographic involvement of metacarpophalangeal and radiocarpal joints in hand osteoarthritis. Clin Rheumatol. 2017;36(5):1077-1082
- Addimanda O, Mancarella L, Dolzani P, Ramonda R, Fioravanti A, Brusi V, Pignotti E, Meliconi R. Clinical associations in patients with hand osteoarthritis. Scand J Rheumatol. 2012;41(4):310-3
- Haugen IK, Bøyesen P. Imaging modalities in hand osteoarthritis—and perspectives of conventional radiography, magnetic resonance imaging, and ultrasonography. Arthritis Res Ther. 2011;13(6):248
- Ramonda R, Frallonardo P, Musacchio E, Vio S, Punzi L. Joint and bone assessment in hand osteoarthritis. Clin Rheumatol. 2014;33(1):11-9).
- Buckland-Wright JC, Verbruggen G, Haraoui PB. Imaging. Radiological assessment of hand OA. Osteoarthritis Cartilage. 2000;8 Suppl A:S55-6).
- Punzi L, Favero M, Frallonardo P, Ramonda R. Time to redefine erosive osteoarthritis. RMD Open. 2015, 25;1(1):e000105
- Punzi L, Frigato M, Frallonardo P, Ramonda R. Inflammatory osteoarthritis of the hand. Best Pract Res Clin Rheumatol. 2010;24(3):301-12
- Punzi L, Ramonda R, Sfriso P. Erosive osteoarthritis. Best Pract Res Clin Rheumatol. 2004;18(5):739-58
- Salaffi F, Ciapetti A, Carotti M. The sources of pain in osteoarthritis: a pathophysiological review. Reumatismo. 2014 6;66(1):57-71
- Rothschild BM. Radiographic assessment of the knee joint in OA. Ann Rheum Dis. 1992;51(12):1345
- Huch K, Kuettner KE, Dieppe P. Osteoarthritis in ankle and knee joints. Semin Arthritis Rheum. 1997;26(4):667-74
- Ornetti P, Brandt K, Hellio-Le Graverand MP, Hochberg M, Hunter DJ, Kloppenburg M, Lane N, Maillefert JF, Mazzuca SA, Spector T, Utard-Wlerick G, Vignon E, Dougados M. OARSI-OMERACT definition of relevant radiological progression in hip/knee osteoarthritis. Osteoarthritis Cartilage. 2009;17(7):856-63).
- Oo WM, Linklater JM, Hunter DJ. Imaging in knee osteoarthritis. Curr Opin Rheumatol. 2017;29(1):86-95
- van Middelkoop M, Bennell KL, Callaghan MJ, Collins NJ, Conaghan PG, Crossley KM, Eijkenboom JJFA, van der Heijden RA, Hinman RS, Hunter DJ, Meuffels DE, Mills K, Oei EHG, Runhaar J, Schiphof D, Stefanik JJ, Bierma-Zeinstra SMA. International patellofemoral osteoarthritis consortium: Consensus statement on the diagnosis, burden, outcome measures, prognosis, risk factors and treatment. Semin Arthritis Rheum. 2018;47(5):666-675
- Filippucci E, Riveros MG, Georgescu D, Salaffi F, Grassi W. Hyaline cartilage involvement in patients with gout and calcium pyrophosphate deposition disease. An ultrasound study. Osteoarthritis Cartilage. 2009;17(2):178-81
- Carotti M, Salaffi F, Di Carlo M, Giovagnoni A. Relationship between magnetic resonance imaging findings, radiological grading, psychological distress and pain in patients with symptomatic knee osteoarthritis. Radiol Med. 2017;122(12):934-943
- Lequesne MG, Maheu E. Clinical and radiological evaluation of hip, knee and hand osteoarthritis. Aging Clin Exp Res. 2003;15(5):380-90
- Siebelt M, Agricola R, Weinans H, Kim YJ. The role of imaging in early hip OA. Osteoarthritis Cartilage. 2014;22(10):1470-80
- Sharma L. Osteoarthritis year in review 2015: clinical. Osteoarthritis Cartilage. 2016;24(1):36-48).
- Jaremko JL, Lambert RGW, Pedersen SJ, Weber U, Lindsay D, Al-Ani Z, Steer K, Pianta M, Wichuk S, Maksymowych WP. OMERACT Hip Inflammation Magnetic Resonance Imaging Scoring System (HIMRISS) Assessment in Longitudinal Study. J Rheumatol. 2019 Feb 15. pii: jrheum.181043. doi: 10.3899/jrheum.181043
- Stelzeneder D, Mamisch TC, Kress I, Domayer SE, Werlen S, Bixby SD, Millis MB, Kim YJ. Patterns of joint damage seen on MRI in early hip osteoarthritis due to structural hip deformities. Osteoarthritis Cartilage. 2012;20(7):661-9
- Feydy A, Pluot E, Guerini H, Drapé JL. Role of imaging in spine, hand, and wrist osteoarthritis. Rheum Dis Clin North Am. 2009;35(3):605-49
- Goode AP, Marshall SW, Renner JB, Carey TS, Kraus VB, Irwin DE, Stürmer T, Jordan JM. Lumbar spine radiographic features and demographic, clinical, and radiographic knee, hip, and hand osteoarthritis. Arthritis Care Res (Hoboken). 2012;64(10):1536-44
- Zhang W, Doherty M, Arden N, Bannwarth B, Bijlsma J, Gunther KP, Hauselmann HJ, Herrero-Beaumont G, Jordan K, Kaklamanis P, Leeb B, Lequesne M, Lohmander S, Mazieres B, Martin-Mola E, Pavelka K, Pendleton A, Punzi L, Swoboda B, Varatojo R, Verbruggen G, Zimmermann-Gorska I, Dougados M; EULAR Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT). EULAR evidence based recommendations for the management of hip osteoarthritis: report of a task force of the EULAR Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT). Ann Rheum Dis. 2005;64(5):669-81
- Salaffi F, Carotti M, Stancati A, Grassi W. Radiographic assessment of osteoarthritis: analysis of disease progression. Aging Clin Exp Res. 2003;15(5):391-404
- Emrani PS, Katz JN, Kessler CL, Reichmann WM, Wright EA, McAlindon TE, Losina E. Joint space narrowing and Kellgren-Lawrence progression in knee osteoarthritis: an analytic literature synthesis. Osteoarthritis Cartilage. 2008;16(8):873-82
- Hellio Le Graverand MP, Clemmer RS, Brunell RM, Hayes CW, Miller CG, Vignon E. Considerations when designing a disease-modifying osteoarthritis drug (DMOAD) trial using radiography. Semin Arthritis Rheum. 2013;43(1):1-8
- Piperno M, Hellio Le Graverand MP, Conrozier T, Bochu M, Mathieu P, Vignon E. Quantitative evaluation of joint space width in femorotibial osteoarthritis: comparison of three radiographic views. Osteoarthritis Cartilage. 1998;6(4):252-9
- Mazzuca SA, Hellio Le Graverand MP, Vignon E, Hunter DJ, Jackson CG, Kraus VB, Link TM, Schnitzer TJ, Vaz A, Charles HC. Performance of a non-fluoroscopicall assisted substitute for the Lyon schuss knee radiograph: quality and reproducibility of positioning and sensitivity to joint space narrowing in osteoarthritic knees. Osteoarthritis Cartilage. 2008;16(12):1555-9
- Vignon E, Piperno M, Le Graverand MP, Mazzuca SA, Brandt KD, Mathieu P, Favret H, Vignon M, Merle-Vincent F, Conrozier T. Measurement of radiographic joint space width in the tibiofemoral compartment of the osteoarthritic knee: comparison of standing anteroposterior and Lyon schuss views. Arthritis Rheum. 2003;48(2):378-84
- Conrozier T, Mathieu P, Piperno M, Provvedini D, Taccoen A, Colson F, Duivon JP, Dusan R, Favret H, Vignon E. Lyon Schuss radiographic view of the knee. Utility of fluoroscopy for the quality of tibial plateau alignment. J Rheumatol. 2004;31(3):584-90
- Riddle DL, Stratford PW, Perera RA. The incident tibiofemoral osteoarthritis with rapid progression phenotype: development and validation of a prognostic prediction rule. Osteoarthritis Cartilage. 2016;24(12):2100-2107
- Niu J, Zhang YQ, Torner J, Nevitt M, Lewis CE, Aliabadi P, Sack B, Clancy M, Sharma L, Felson DT. Is obesity a risk factor for progressive radiographic knee osteoarthritis? Arthritis Rheum. 2009, 15;61(3):329-35
- Kinds MB, Marijnissen AC, Vincken KL, Viergever MA, Drossaers-Bakker KW, Bijlsma JW, Bierma-Zeinstra SM, Welsing PM, Lafeber FP. Evaluation of separate quantitative radiographic features adds to the prediction of incident radiographic osteoarthritis in individuals with recent onset of knee pain: 5-year follow-up in the CHECK cohort. Osteoarthritis Cartilage. 2012;20(6):548-56
- Karsdal MA, Bihlet A, Byrjalsen I, Alexandersen P, Ladel C, Michaels M, Andersen JR, Riis BJ, Kraus V, Bay-Jensen AC, Christiansen C. OA phenotypes, rather than disease stage, drive structural progression–identification of structural progressors from 2 phase III randomized clinical studies with symptomatic knee OA. Osteoarthritis Cartilage. 2015;23(4):550-8
