GLI INDICATORI SOGGETTIVI DI VALUTAZIONE DELL’ESITO IN REUMATOLOGIA: RUOLO DEI PATIENT-REPORTED OUTCOMES
AUTORI:
1Clinica Reumatologica Ospedale “Carlo Urbani”, Dipartimento Scienze Cliniche e Molecolari Università Politecnica delle Marche, Jesi, Ancona
Introduzione
La misurazione delle prestazioni o degli esiti, associata ad un qualsiasi processo in ambito sanitario si può realizzare attraverso un sistema di indicatori predefiniti che forniscono elementi omogenei (quantitativi, qualitativi, di outcome, ecc.) e garantiscono il giusto livello di oggettività della valutazione e la necessaria “correttezza” della metodologia seguita. Gli indicatori sono definibili come‚ “informazioni selezionate allo scopo di conoscere fenomeni di interesse, misurandone i cambiamenti e, conseguentemente, contribuendo ad orientare i processi decisionali” (Ministero della Salute, decreto 12/12/2001 pubblicato sul Suppl. Ord. N° 34 alla GURI del 09/02/2012). La qualità della misurazione si basa sulla disponibilità di indicatori appropriati e di dati corretti e tempestivi che alimentano gli indicatori, in maniera tale da consentire di programmare e mettere in atto le decisioni terapeutiche correttive, in ogni fase del “monitoraggio intensivo” (tight control). Gli indicatori di risultato o di esito, in particolare, possono essere di non immediata rilevazione per le caratteristiche di lenta evoluzione del quadro clinico articolare e per la variabilità della malattia. Una loro difficile interpretabilità può, inoltre, essere correlata a fattori culturali, socio-ambientali o a fattori non direttamente sotto il controllo diretto del medico (aderenza al trattamento, ecc). Per adempiere la propria funzione un buon indicatore di esito deve assolvere ad una serie di caratteristiche riportate nella Tabella 1.
Patient-reported outcomes
La classificazione internazionale del Funzionamento delle Disabilità e della Salute (ICF) riflette i cambiamenti di prospettiva nella disabilità maturati nel corso degli ultimi decenni, enunciati nei seguenti tre principi fondamentali: universalismo, approccio integrato, modello interattivo e multidimensionale del funzionamento e della disabilità. Si tratta di un capovolgimento di logica: mentre gli indicatori tradizionali si basano sui tassi di mortalità, l’ICF pone come punto centrale la “qualità della vita” delle persone affette da malattie. Il riconoscimento della capacità di autopercezione degli effetti degli interventi di assistenza sanitaria e dell’impatto della malattia cronica sullo stato di salute, ha favorito lo sviluppo di indicatori soggettivi dell’esito, denominati (Patient-Reported Outcomes – PROs). Nell’ambito, sia della pratica clinica quotidiana, che della ricerca, l’impiego di tali indicatori è largamente diffuso e condiviso in Reumatologia, persino in misura superiore ad altre discipline medico-chirurgiche. La Food and Drug Administration (FDA) ha definito estensivamente i PROs come “any report coming from patients about a health condition and its treatment”. Fanno parte dei PROs gli usuali strumenti per la misura della disabilità fisica e della qualità della vita che esplorano i sintomi correlati alla malattia (dolore, fatica, qualità del sonno), oltre alla funzionalità ed al benessere psico-fisico. Appartengono ai PROs, inoltre, tutti i report riferiti dal paziente in merito ai comportamenti di salute, quali la sua adesione alla cura, il mutamento rilevante dei suoi stili di vita dovuto alla malattia, la partecipazione a programmi riabilitativi. Infine, possono essere considerati PROs anche l’espressione delle preferenze di cura del paziente ed il suo desiderio di partecipare (o meno) al processo terapeutico, la sua soddisfazione per le cure, le sue valutazioni della qualità di comunicazione medico/paziente e la facilità di accesso alle cure. I PROs forniscono, pertanto, informazioni non disponibili da altre fonti, e ciò assume particolare valore, in quanto la prospettiva dei pazienti sulla malattia è, assai spesso, diversa dal punto di vista del medico. I PROs permettono di descrivere, misurare e valutare lo stato di attività di malattia attraverso la percezione della propria condizione di salute, fornendo una maggiore attendibilità alla valutazione complessiva dello stato di benessere. I PROs contribuiscono anche a migliorare le conoscenze sulla storia naturale della malattia. I benefici sono evidenti: maggiore tempestività nel management dei sintomi, minore ansietà del paziente, minor ricorso alle cure ospedaliere, maggior adesione del paziente ai consigli del medico, maggiore soddisfazione con le cure, più efficace uso delle risorse e complessivo snellimento del processo di “decision-making”. L’impiego di tali indicatori di valutazione soggettiva dell’esito, ha reso disponibile una pluralità di indicatori (PRO-Indices) di rapido e facile utilizzo. I PROs sono utilizzati con sempre maggiore frequenza nella valutazione di nuovi farmaci e nella valutazione della qualità della vita dei pazienti reumatici. Nel 2006 l’agenzia americana “Food and Drug Administration” (FDA) ha redatto una normativa relativa allo sviluppo ed all’approvazione di nuovi farmaci che prevede espressamente l’utilizzo dei PROs.
Definizione della qualità della vita
Il concetto di qualità della vita è molto antico. Epicuro, nel IV secolo avanti Cristo, nella lettera, a Meneceo, scrisse: “una salda conoscenza dei bisogni inclina a ricondurre ogni assenso o diniego al benessere del corpo ed alla piena serenità dell’animo, poichè questo è il fine della vita felice. A questo fine noi rivolgiamo ogni nostra azione, per allontanarci dalla sofferenza e dall’apprensione”. Nonostante ciò, in medicina, il concetto di qualità di vita come entità misurabile e della misurazione della qualità di vita come strumento utilizzabile in sociologia, è relativamente recente. L’OMS nel 1947 definisce lo stato di salute (non è ancora presente il concetto di qualità di vita) come: “completo benessere fisico, mentale e sociale e non una mera assenza di malattia ed infermità”. Nel 1993 la stessa organizzazione, descrivendo la qualità di vita, fornisce la seguente definizione: “la percezione dell’individuo della sua posizione nella vita nel contesto della cultura e del sistema di valori in cui vive ed in relazione ai suoi obiettivi, alle sue aspettative, ai suoi modelli e rapporti”. Da tali definizioni si può comprendere come la qualità della vita sia una struttura complessa che deve tener conto dell’età di un individuo, della sua cultura, del suo grado di istruzione, del suo reddito, delle sue aspettative e dei contesti sociale, ambientale e familiare in cui vive. Da quando l’OMS ha modificato la definizione di salute (Constitution of the World Health Association, 1952), il concetto di qualità di vita ha trasceso l’idea di un indicatore sintetico degli esiti delle malattie ed è diventato un parametro fondamentale della salute individuale e collettiva, da cui non si può prescindere per ogni valutazione sanitaria. Vi è stato un incremento esponenziale dell’interesse per questo aspetto della valutazione medica. In particolare, nei paesi economicamente avanzati si è sviluppata l’attenzione alla qualità di vita e alla sua misurazione. La definizione oggi condivisa di “qualità di vita” si riferisce al concetto di “qualità di vita correlata alla salute” (Health-Reated Quality of Life – HRQOL), poichè meglio descrive ciò che collettivamente percepiamo della salute in rapporto ad uno stato morboso. Secondo la definizione di Marcia A. Testa, il termine di qualità della vita correlata alla salute si riferisce “all’insieme della dimensione fisica, psicologica e sociale della salute, viste come aree distinte, influenzate da esperienze, convinzioni, aspettative e sensazioni del soggetto”. Ciascuna di queste dimensioni può essere misurata secondo due prospettive: la valutazione oggettiva dello stato di salute (corrispondente all’asse delle ordinate e la percezione soggettiva della salute (corrispondente all’asse delle ordinate all’asse delle ascisse nella Figura 1.
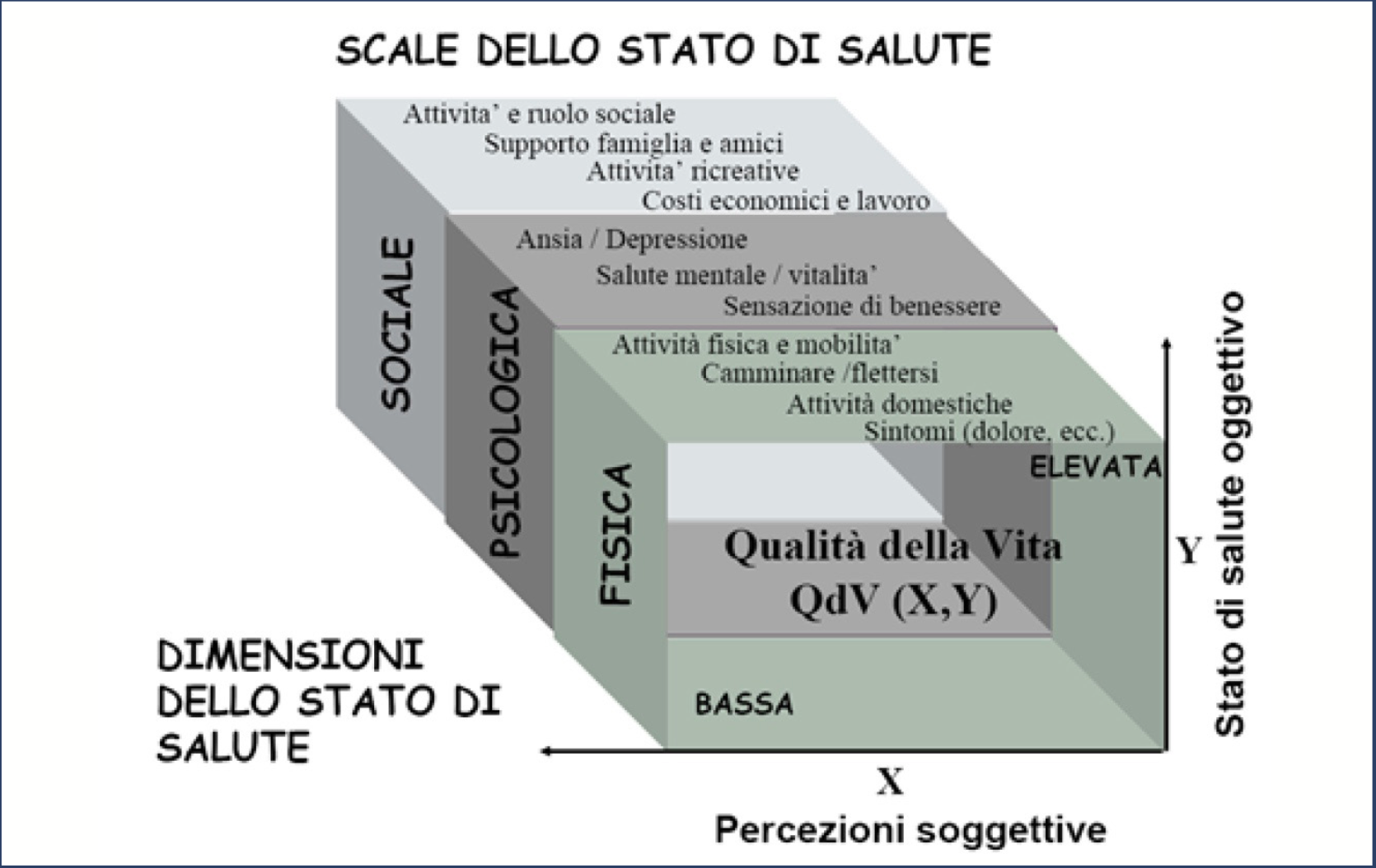 Figura 1. Dimensioni dello stato di salute e quantificazione dei domini (riprodotta da Salaffi F. Carotti M. Valutazione della disabilità e della qualità della viita nelle malattie muscolo scheletriche. In Clinimetria delle Malattie Muscoloscheletriche. Edizione Mattioli 1885, Fidenza 2007, capitolo 2; pp 61).
Figura 1. Dimensioni dello stato di salute e quantificazione dei domini (riprodotta da Salaffi F. Carotti M. Valutazione della disabilità e della qualità della viita nelle malattie muscolo scheletriche. In Clinimetria delle Malattie Muscoloscheletriche. Edizione Mattioli 1885, Fidenza 2007, capitolo 2; pp 61).
Valutazione della qualità della vita
La valutazione della qualità della vita nelle malattie muscoloscheletriche è considerata un elemento di importanza strategica, non solo in ambito valutativo, ma anche in chiave prognostica. Il riconoscimento della capacità di autopercezione degli effetti degli interventi di assistenza sanitaria e dell’impatto della malattia cronica sullo stato di salute, ha favorito lo sviluppo di scale e di questionari, che hanno trovato un crescente impiego in reumatologia, soprattutto nell’artrite reumatoide. La natura progressiva e invalidante di numerose malattie muscoloscheletriche, in particolare dell’artrite reumatoide, impatta in maniera significativa sulla qualità della vita e sulla capacità lavorativa di coloro che ne sono affetti. Ciò comporta l’esigenza di una valutazione globale dello stato di salute del paziente che tenga conto, non solo delle caratteristiche clinico-biologiche della malattia, ma anche dei potenziali esiti. Appare, quindi, evidente che il riuscire ad individuare i livelli di inibizione funzionale e comportamentale, determinati dalla malattia sullo stato globale di salute, può risultare di aiuto nell’approntare una serie di programmi (schemi farmacologici, tecniche di economia articolare, strategie cognitive nell’affrontare i problemi ecc.), volti ad un maggiore coinvolgimento dei pazienti nella gestione della propria salute (Figura 2).
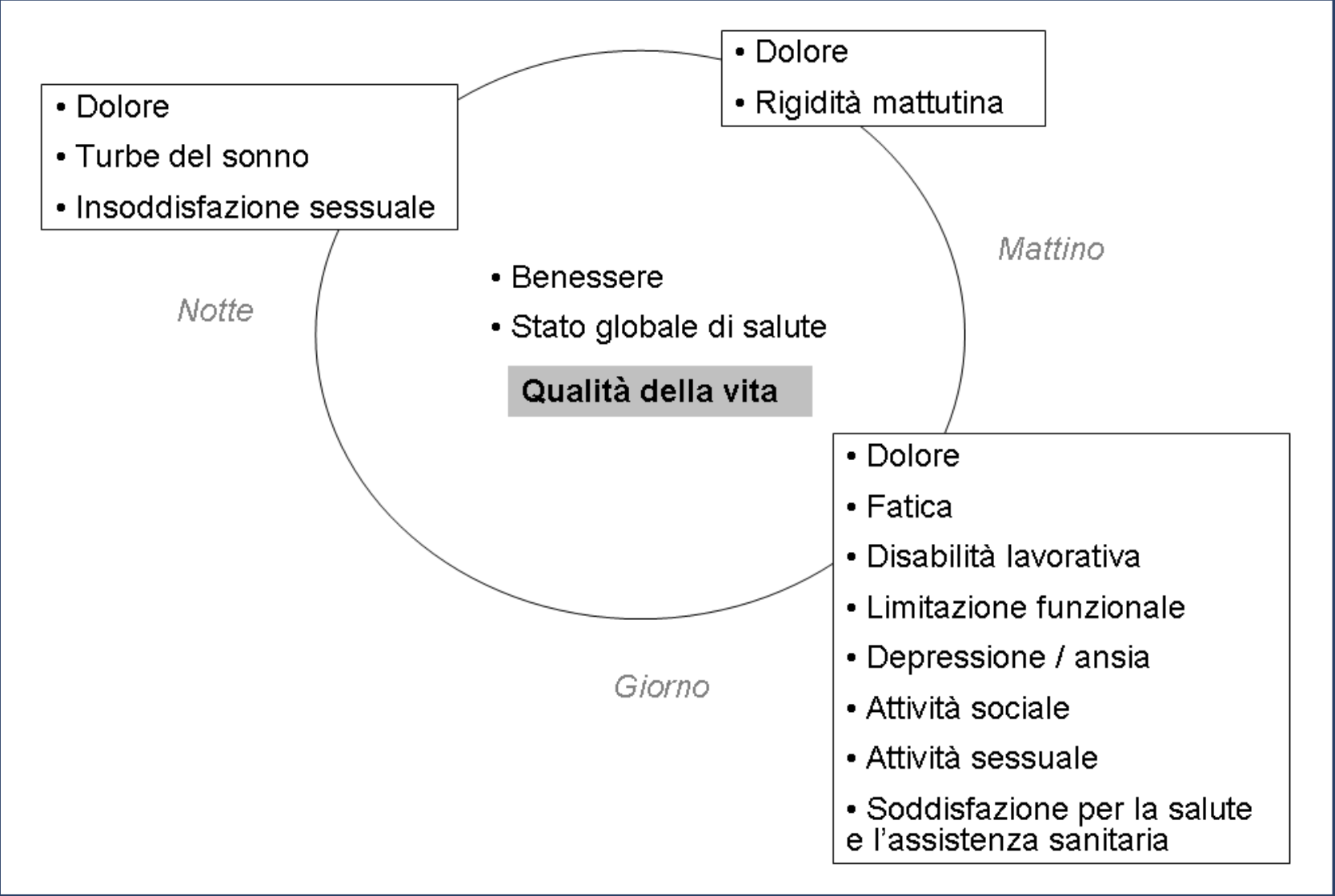 Figura 2. Domini considerati rilevanti da parte del paziente in corso di artrite reumatoide.
Figura 2. Domini considerati rilevanti da parte del paziente in corso di artrite reumatoide.
Và oggi riconosciuta l’opportunità di una classificazione schematica degli studi sulla qualità della vita che identifica due tipologie di studi: 1° tipologia: studi descrittivi finalizzati ad una misurazione analitica della qualità della vita e privi di implicazioni economiche; 2° tipologia: studi finalizzati alla misurazione della qualità della vita mediante la tecnica della “utilità e connessi ad analisi economiche sui costi verso i benefici. La prima di queste due tipologie riflette un’impostazione tradizionale del disegno clinico dello studio. La finalità della ricerca è, in generale, analitico-descrittiva e l’obiettivo principale è quello di scomporre la qualità della vita nelle sue molteplici componenti (quantificando ciascuna di esse con opportuni indici numerici). Ulteriori obiettivi di questo tipo di ricerca sono la stima dell’impatto della malattia sulle condizioni generali di salute, oppure la valutazione degli effetti di un intervento terapeutico sulla qualità della vita stessa. Questo versante di ricerca non ha implicazioni economiche e, quindi, non mette in rapporto i dati relativi alla qualità della vita (ad es. l’esito del trattamento) con il costo della terapia. La seconda tipologia di studi si basa, invece, su un’impostazione metodologica riassuntiva; lo scopo è quello di sintetizzare i diversi aspetti della qualità della vita con un unico dato numerico (il quale è costituito dal valore della “utilità” e cioè da un numero compreso tra 0 ed 1, dove 0 rappresenta la morte ed 1 rappresenta la salute perfetta). In generale, il valore dell’utilità viene utilizzato come fattore di moltiplicazione nei confronti degli anni di vita vissuti. Questa moltiplicazione, applicata preferibilmente sui dati individuali del paziente, ha lo scopo di “pesare” la quantità della sopravvivenza in funzione della qualità della sopravvivenza stessa, generando, in tal modo, i cosiddetti “quality-adjusted life years” (QALYs).
Tappe metodologiche nello sviluppo di un questionario di valutazione della qualita’ della vita
In biomedicina, il passaggio da una ricerca meramente “descrittiva” ad una ricerca “quantitativa” è avvenuto recentemente e solo da allora si è affermata la necessità di misurare e descrivere, con modelli matematici, i fenomeni biologici. Attualmente, la quantificazione dei sintomi, del quadro clinico e dei suoi possibili esiti, anche in termini di impatto sullo stato generale di salute, è un prerequisito dal quale non può sottrarsi alcun ricercatore. I questionari rappresentano uno strumento quantitativo per rilevare le percezioni e i livelli di soddisfazione di un insieme di pazienti, che hanno fruito di un servizio sanitario, in modo economico, veloce e anonimo. Tali strumenti permettono di realizzare sia confronti diacronici, che rilevano i cambiamenti nel tempo (finalità valutativa) dei livelli di soddisfazione dei pazienti, sia sincronici tra livelli di soddisfazione relativi a servizi simili (finalità discriminativa). Sono “strumenti di raccolta delle informazioni, definiti come un insieme strutturato di domande e relative categorie di risposta definite a priori da chi lo costruisce, ovvero di domande cosiddette “chiuse” dove all’intervistato viene richiesto di individuare tra le risposte presentate quella che più si avvicina alla propria posizione, e/o di domande “aperte”, che non prevedono cioè delle risposte predeterminate”, ma alle quali il soggetto può rispondere riportando e valutando la propria esperienza” (Tabella 2). Le fasi di attribuzione dei punteggi (ricodifica dei valori delle risposte date e di quelle mancanti, inversioni dei punteggi e/o ricalibrazione dei punteggi dei quesiti, calcolo dei punteggi grezzi di scala, trasformazione dei punteggi “grezzi” e costruzione di indici sintetici basati su standard di riferimento ricavati da popolazioni di controllo) vengono, di norma, eseguiti con l’ausilio di un computer, utilizzando gli algoritmi e le griglie di calcolo suggeriti dai vari manuali d’uso ai questionari o mediante programmi “software”, altrimenti disponibili.
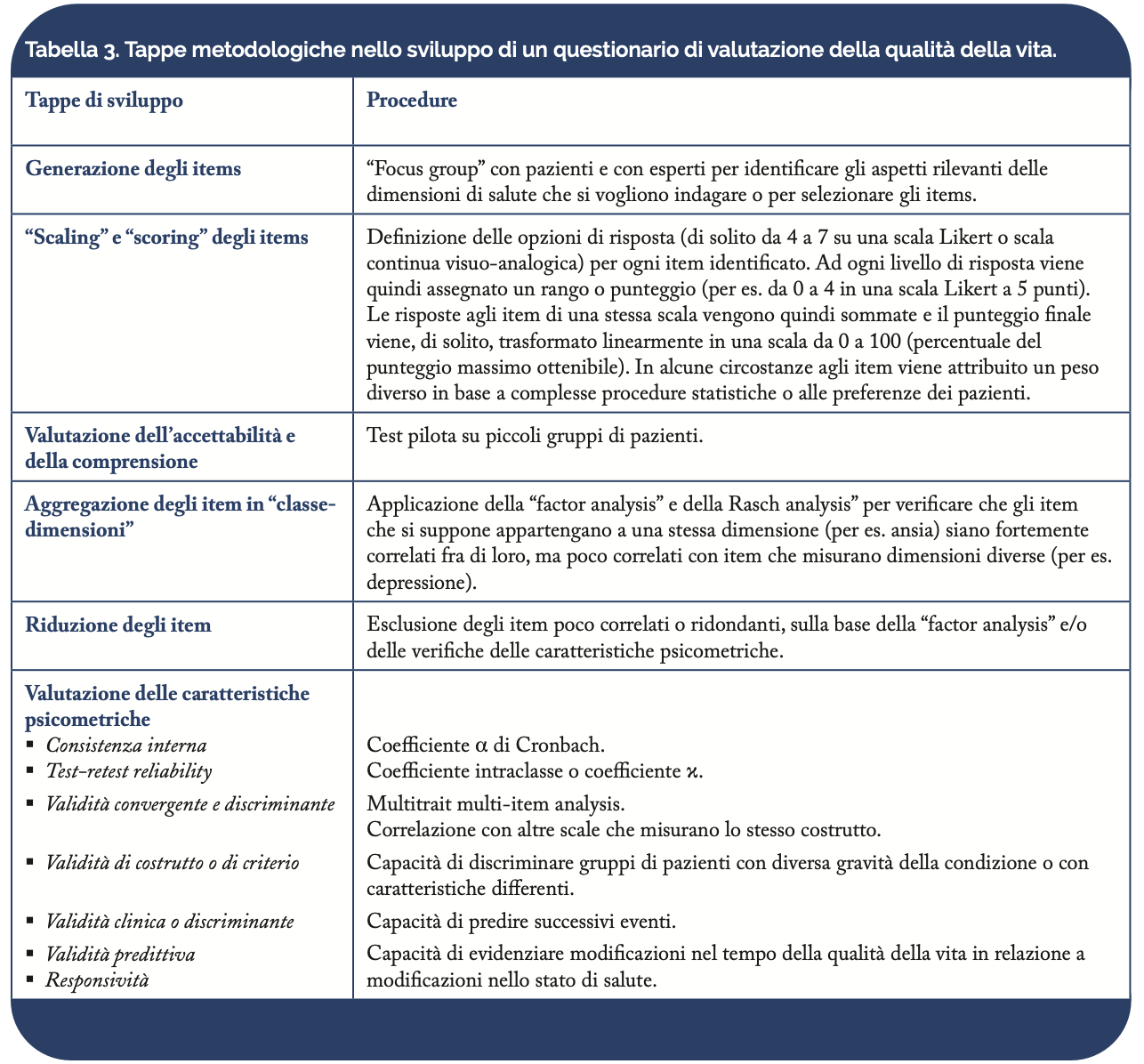
La validazione di un questionario o di una scala di valutazione si può basare sull’utilizzo di strumenti precedentemente sviluppati e validati. In assenza di uno strumento disponibile, lo sviluppo di un nuovo questionario di valutazione è necessario e ciò richiede un processo che, solitamente, avviene secondo delle fasi prestabilite: (i) identificazione di una specifica popolazione di pazienti, (ii) selezione degli items, (iii) riduzione degli items, (iv) studio di validazione (Tabella 3).
La prima fase consiste nella identificazione della popolazione “target”, al fine di sviluppare uno strumento specifico per la valutazione della malattia. La revisione della letteratura consente di selezionare gli “items” considerati utili per la valutazione e da includere nello strumento finale. La generazione degli “items” si basa generalmente sul lavoro a gruppi (“focus group”) tra pazienti ed esperti per identificare gli aspetti rilevanti delle dimensioni che si vogliono indagare. Successivamente, gli “items” selezionati vengono ridotti di numero al fine di ottenere uno strumento finale che sia di facile e semplice utilizzo. L’impiego dello strumento in corso di uno studio pilota su piccoli gruppi di pazienti permette, in seguito, di valutarne l’accettabilità e la comprensione. Successivamente, per ogni questionario che si prospetta di uso clinico, occore un’attenta verifica delle principali caratteristiche psicometriche, quali la validità, l’affidabilità e la responsività.
Caratteristiche psicometriche di un questionario di valutazione della qualita’ della vita
VALIDITA’
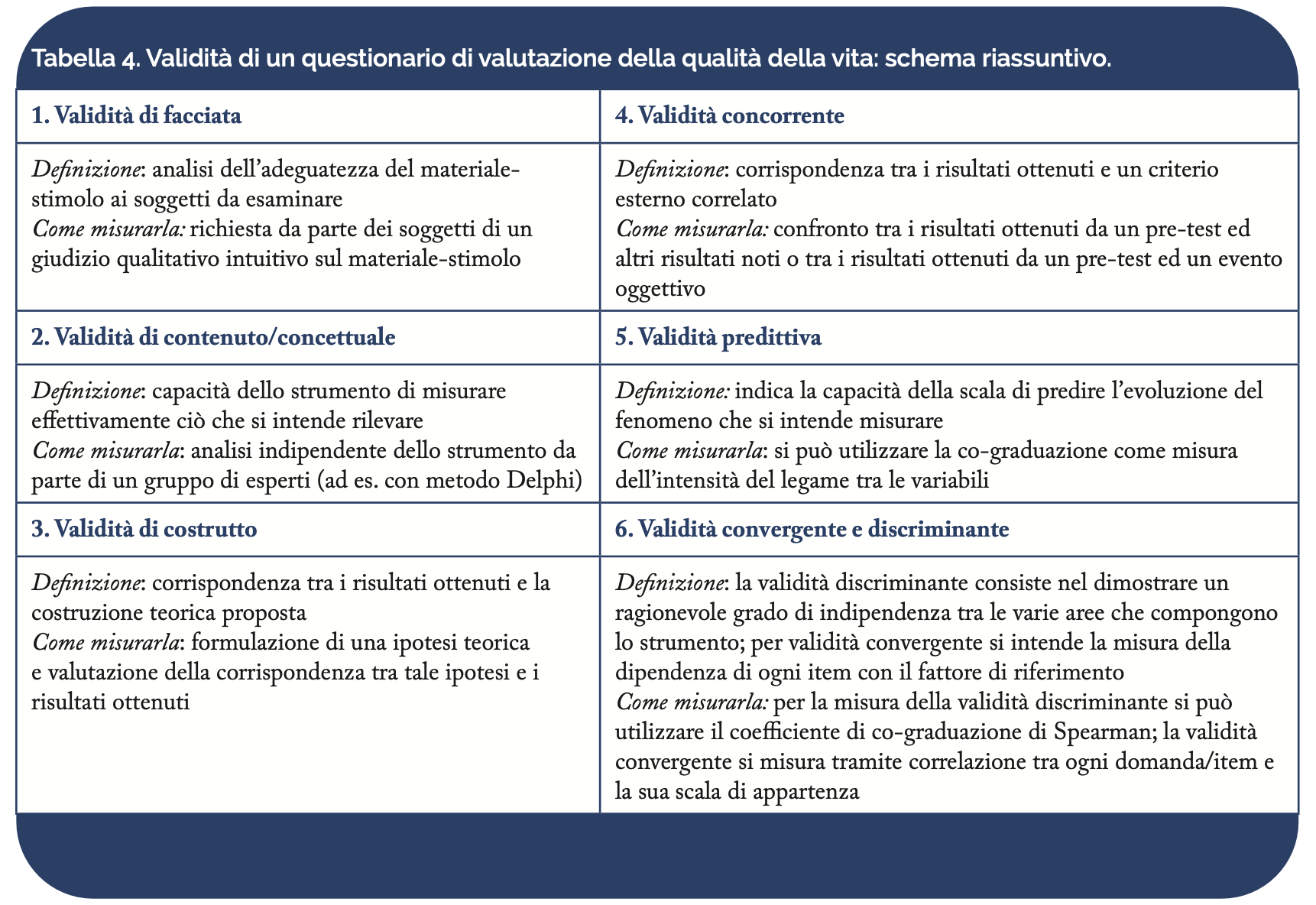
La validità (validity) si riferisce alla proprietà del giudizio clinico di dimostrarsi in accordo con evidenze più probanti, quale un più attento esame obiettivo o strumentale del paziente, o la sua osservazione nel corso del tempo (gold standard). La validità viene tradizionalmente distinta in: validità di criterio o di facciata (face validity), validità di contenuto o concettuale (content validity), di costrutto (construct validity), di criterio (criterion/predictive validity) e in valdità concorrente (concurrent validity), convergente (convergent validity) e discriminante (discriminant validity) (Tabella 4).La validità (validity) si riferisce alla proprietà del giudizio clinico di dimostrarsi in accordo con evidenze più probanti, quale un più attento esame obiettivo o strumentale del paziente, o la sua osservazione nel corso del tempo (gold standard). La validità viene tradizionalmente distinta in: validità di criterio o di facciata (face validity), validità di contenuto o concettuale (content validity), di costrutto (construct validity), di criterio (criterion/predictive validity) e in valdità concorrente (concurrent validity), convergente (convergent validity) e discriminante (discriminant validity) (Tabella 4).
a. Face Validity: si tratta di una caratteristica del test non propriamente metrologica, né facilmente quantificabile. In pratica, l’esame della validità di facciata si riduce ad un giudizio qualitativo, intuitivo sull’adeguatezza del materiale-stimolo ai soggetti da esaminare.
b. Content Validity: la validità di contenuto o concettuale denota l’adeguatezza della teorizzazione e definizione di tutte le variabili misurate in una certa ricerca. Ciò è importante, in quanto uno stesso concetto può essere misurato in modi diversi a seconda degli scopi dell’indagine e a seconda della teoria o conoscenza di quel fenomeno, ed è dunque la congruenza, tra questa molteplicità di fatti, che può garantire la validità di costrutto o di contenuto. Per misurare la validità di contenuto è possibile sottoporre lo strumento a un gruppo di esperti per un’analisi indipendente. Ad esempio, è possibile utilizzare il metodo Delphi, che si basa su un processo strutturato che raccoglie informazioni dal patrimonio conoscitivo di un gruppo di esperti, con lo scopo di approfondire risposte individuali al problema posto, aiutando gli esperti ad affinare progressivamente il loro punto di vista, mano a mano che il gruppo progredisce nella riflessione.
c. Construct Validity: la validità di costrutto riguarda le teorie a cui si fa riferimento per la costruzione dello strumento, quali concettualizzazioni si usano e quali misure si costruiscono per le variabili a cui si è interessati. È quindi una corrispondenza tra i risultati ottenuti e la costruzione teorica proposta. La validità di costrutto è verificata attraverso la misura della correlazione tra un indicatore ed altri indicatori secondo particolari modelli teorici.
d. Criterion Validity / Predictive Validity: rappresenta la capacità di uno strumento di fare previsioni accurate. La verifica di tale validità è fatta a partire dalla sua adeguatezza nel predire un criterio esterno, da cui il nome.
e. Concurrent Validity: è determinata osservando quanto lo strumento correla con altri strumenti che il ricercatore ritiene validi nel misurare la stessa caratteristica. L’osservazione di una relazione statisticamente significativa è considerata verifica della validità.
f. Convergent Validity: è determinata confrontando e correlando i punteggi ottenuti con la misura da validare con quelli ottenuti con la misura di un altro costrutto, teoricamente legato al primo. La possibilità di verificare la validità convergente dipende, quindi, dall’esistenza di costrutti, e relative misure, legati con quello misurato.
g. Discriminant Validity: è speculare alla validità convergente; essa è alta quando la misura da validare non correla con le misure di altri costrutti, teoricamente distinti dal primo.
AFFIDABILITA’
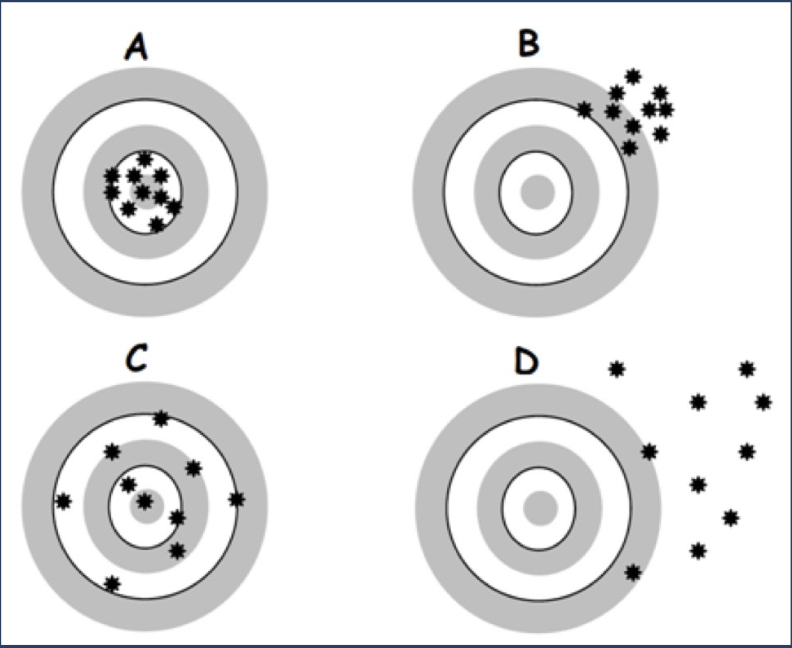
Il secondo requisito che una scala di misura deve soddisfare nella costruzione di un test è l’affidabilità. In statistica, l’affidabilità esprime la costanza di un insieme di misure o di un particolare strumento di misura. Una misurazione è affidabile se i risultati rimangono costanti allo stesso modo nel tempo. In questo caso si avrà un’alta affidabilità, mentre uno strumento di misura non è affidabile se le misure ripetute forniscono risultati differenti, nonostante non vi siano cambiamenti evidenti nei soggetti esaminati. Uno strumento viene definito tanto affidabile quanto meno la misura è sensibile all’errore casuale. Per descrivere l’affidabilità delle misure si usano spesso i termini accuratezza e precisione. L’accuratezza rappresenta il grado di conformità di una quantità misurata/calcolata al suo reale e vero valore e quindi, descrive la capacità di un sistema di misurazione di avvicinarsi ad un valore accettato: più si avvicina a tale valore maggiore è la sua accuratezza. Valutare l’accuratezza richiede la contemporanea osservazione di un processo noto o la disponibilità di un valore di riferimento (calibrazione). La precisione rappresenta il grado in cui misurazioni successive mostrano lo stesso risultato o risultati simili. Mediante la determinazione della precisione di uno strumento è possibile verificare, quindi, la capacità di misurare con il minor grado di distorsione possibile. La precisione è correlata ai concetti di robustezza e stabilità e può essere distinta in ripetibilità (ovvero la variazione prodotta quando si sono fatti tutti gli sforzi per mantenere costanti le condizioni di misurazione attraverso ripetizioni entro poco tempo) e riproducibilità (ovvero la variazione prodotta utilizzando lo stesso procedimento di misurazione con strumenti e operatori diversi anche con intervalli di tempo lunghi). Per chiarire entrambi i concetti può essere utile far riferimento alla nota analogia delle frecce lanciate contro un bersaglio: quando tutte le frecce occupano un’area molto ristretta, la misurazione è considerata precisa. La dimensione dell’area colpita dalle frecce è interpretata come “grado di precisione”. Quando le frecce si posizionano molto vicine al centro sono considerate accurate. La distanza del gruppo di frecce dal centro è interpretata come “livello di accuratezza”. In altre parole, più la procedura di misurazione produce valori vicini a quello atteso, più accurata è la procedura. Gli esempi, riportati di seguito, mostrano gruppi di misure ripetute che sono abbastanza accurate e precise (Figura 3-A), precise ma non accurate (Figura 3-B), imprecise e non accurate (Figure 3-C e D). L’affidabilità delle misurazioni ottenute mediante i questionari è parte integrante delle verifiche empiriche sulla validità. Tali verifiche riguardano la consistenza o coerenza interna [grado di inter-correlazione fra i quesiti costituenti le singole sottoscale del questionario (item-internal consistency) e fra i singoli quesiti e le diverse sottoscale (item-discriminant validity)], la riproducibilità inter-esaminatore (grado al quale i punteggi ottenuti da un esaminatore sono sovrapponibili a quelli registrati da un secondo esaminatore), la riproducibilità intra-esaminatore (grado al quale i punteggi ottenuti da un esaminatore in una determinata circostanza sono sovrapponibili con quelli ottenuti quando lo stesso esaminatore riapplica la stessa misura in un tempo successivo) e la riproducibilità al test-retest (grado di variabilità dei punteggi a seguito di misurazioni ripetute in condizioni analoghe).
Figura 3.Rappresentazione simbolica di precisione e accuratezza rispetto al centro del bersaglio
Per coerenza interna o omogeneità degli stimoli si intende la corrispondenza tra le risposte all’interno dello strumento. La formula di tipo generale attualmente più utilizzata in psicometria per calcolare l’indice di consistenza o coerenza interna è quella definita da Cronbach come “indice alfa”. Per calcolare questo indice occorre eseguire una correlazione tra gli item dello stesso test; ciò è possibile utilizzando una formula manuale o con il supporto di alcuni programmi informatici come Excel, SPSS o MEDCALC. I valori che l’alfa di Cronbach può assumere oscillano tra 0 e 1, dove i valori tendenti a 0 indicano una bassa correlazione, mentre i valori tendenti a 1 ipotizzano una forte correlazione, indice di omogeneità degli item. Un altro metodo per calcolare i coefficienti di attendibilità utilizza stime che non sfruttano tutta l’informazione disponibile item per item. Tra questi i più diffusi sono i coefficienti ottenuti con il metodo “split half” (divisione a metà) e corretti con la formula di Spearman-Brown. La fedeltà nel tempo di uno strumento, detta anche stabilità, si misura con il metodo test re-test, in base al quale lo stesso strumento viene somministrato in due distinte occasioni separate tra loro da un intervallo di tempo sufficientemente ampio da far sì che le risposte, date nella seconda misurazione, non si possano basare sul ricordo delle risposte date nella prima misurazione. Se le risposte date nelle due occasioni sono significativamente simili tra loro, cioè sono altamente correlate, lo strumento è fedele. Per quantificare la correlazione fra misure costituite da variabili continue o razionali, distribuite normalmente, viene comunemente impiegato il coefficiente di correlazione r di Pearson. Se le variabili non mostrano una distribuzione “normale” si preferisce ricorrere ad un test non parametrico, quale il coefficiente di correlazione per ranghi di Spearman. La riproducibilità per dati ordinali viene comunemente quantificata dal coefficiente kappa (k): il suo massimo valore è 1, quando l’accordo fra misure ripetute è perfetto. Un valore pari a 0 significa non accordo al di là della casualità. Anche se le dimensioni di kappa dipendono da altri fattori oltre la riproducibilità, un kappa inferiore a 0,40 è considerato basso (scarsa riproducibilità), superiore a 0,80 è considerato molto buono. Un metodo alternativo di valutare la riproducibilità di punteggi su scale ordinali è la stima del coefficiente di correlazione intra-classe, mediante il calcolo della varianza. Anche in questo caso, il range dei valori è compreso fra 0 (non riproducibilità) e 1 (varianza dovuta interamente alla variabilità fra soggetti).
RESPONSIVITA’
Per uno strumento con finalità valutative, designato cioè a monitorare nel paziente le variazioni dello stato di salute, è fondamentale la verifica della responsività (o sensibilità ai cambiamenti). La responsività rappresenta la proprietà psicometrica più rilevante di uno strumento di misura, anche per le dirette implicazioni inerenti la determinazione della numerosità campionaria (errore di tipo II). Operativamente, la responsività (meglio nota come “responsiveness”) di un questionario o di una dimensione da esso esplorata, può essere definita come la capacità di una misura di rilevare con precisione un cambiamento significativo nell’intervallo di tempo considerato (ad esempio osservando i cambiamenti della misura prima e dopo un trattamento efficace con farmaci biologici nell’artrite reumatoide). Esistono due tipi principali di responsività: interna ed esterna. Per responsività interna si intende la capacità di una misura o di un gruppo di misure di rilevare un cambiamento nel tempo in risposta ad un intervento. La responsività interna è di solito valutata nel contesto di studi clinici o in presenza di ripetuti provvedimenti e dipende dal tipo di intervento e dagli outcome considerati per determinarne l’efficacia. Sebbene non vi sia unanime accordo circa l’approccio ottimale alla misurazione della responsività interna, la stima dell’Effect Size (ES) ed il calcolo dello Standardized Response Mean (SRM) raccolgono i maggiori consensi. L’ES è definito come il rapporto fra la variazione media dei punteggi rilevati al basale ed al termine del follow-up con la deviazione standard (DS) del punteggio rilevato al basale. L’SRM è definita come il rapporto fra la variazione media dei punteggi rilevati al basale ed al termine del follow-up, con la DS della variazione media di tali punteggi. Elevati valori di SRM e ES indicano una maggiore sensibilità nel cogliere le variazioni dello stato di salute. In particolare, valori di 0,2, 0,5, e 0,8 o superiori corrispondono, rispettivamente, ad una bassa, moderata o elevata responsività. La responsività esterna, invece, riflette l’associazione tra variazioni individuali di una misura nel tempo e corrispondenti variazioni individuali di una misura esterna “di riferimento” dello stato di salute. Tale analisi consente di quantificare l’entità del cambiamento in base al riferimento esterno. Per questo motivo, a differenza della responsività interna, la responsività esterna non dipende dall’intervento e/o dalla misura utilizzata, ma piuttosto dalla scelta del riferimento esterno. L’analisi delle curve operative Receiver Operating Characteristic (ROC) è il metodo più spesso utilizzato per valutare la responsività esterna. Le proprietà delle curve ROC consentono di valutare la performance di un test diagnostico basato su valori soglia in modo semplice, efficace e costruito su una consolidata teoria statistica e di eseguire confronti tra test diversi. Con le curve ROC si suddivide il campo di variabili di un test in piccoli intervalli nei quali si analizza la sensibilità e la specificità del test in esame. Tali dati vengono poi riportati, rispettivamente, sull’asse delle ordinate e delle ascisse in un sistema di assi cartesiani. I punti così ottenuti, per ogni intervallo di frequenza, vengono congiunti da un’unica linea, in modo da costruire la ROC del test. Il test, la cui ROC sottende l’area maggiore, viene considerato come il più responsivo. Se l’area sottesa alla curva ROC non supera il valore della bisettrice degli assi cartesiani (cioè il 50% dell’area massima ottenibile, e cioè 1) si può dedurre che il test non è applicabile per le finalità per le quali è stato utilizzato.
Metodi di somministrazione dei questionari
L’esito finale dei PROs, che prevede la somministrazione di questionari, può essere influenzato da diversi elementi, tra cui figura, principalmente, la modalità di raccolta dei dati (Tabella 5).
Alcuni comportamenti possono, tuttavia, essere adottati dal medico in fase di valutazione, al fine di minimizzare la possibilità di generare distorsioni o “bias” nella raccolta delle informazioni (Tabella 6). La compilazione di questionari, mediante l’utilizzo di personal computer o altri strumenti elettronici (Smartphone, Tablet PC), consente una migliore raccolta dei dati sensibili, in quanto considerata, dai pazienti, una modalità più anonima rispetto all’uso convenzionale con carta e penna/matita. La lettura del consenso informato, prima ancora della compilazione del questionario, può avere, allo stesso modo, un favorevole impatto sui risultati dell’autovalutazione. I pazienti più consapevoli dei rischi di divulgazione dei dati sensibili tendono generalmente a fornire minori informazioni. Il contesto, inoltre, in cui sono raccolti i PROs può influenzare l’esito della raccolta dati, mentre l’affidabilità e la validità di tali dati dipende dalla chiarezza, precisione e comprensione della domanda e dalla capacità, da parte del paziente, di generare una precisa e obiettiva risposta.
La risposta ad ogni singola domanda richiede una serie complessa di operazioni cognitive tra cui figurano:
- ricordo: richiamo del sintomo “target” o evento in questione (tale da implicare enumerazione delle molte occasioni nel corso di un periodo di tempo considerevole);
- ancoraggio: richiamo dell’evento o sintomo riferito ad un preciso periodo di tempo;
- aggregazione: esperienza del sintomo nel corso del tempo (media numerica degli eventi per il periodo di tempo considerato).
È noto che la rievocazione del sintomo in memoria non è un semplice recupero di un evento, ma si basa su una varietà di passaggi mentali ed una ricostruzione retrospettiva, a volte imperfetta e soggetta ad una serie di pregiudizi, necessarie per rispondere. Ogni fase del processo di elaborazione, di fatto, ha il potenziale per introdurre imprecisioni e distorsioni o “bias” nella raccolta dei dati. Esiste, inoltre, una forte evidenza che la memoria per gli eventi sia subordinata ad un effetto denominato “telescoping”, ovvero la tendenza a portare avanti nel tempo eventi passati ed “avvicinarli” al momento attuale. L’aggregazione di più esperienze, una volta ricordate, è anch’essa fonte di potenziali “bias”. Tale tipo di elaborazione cognitiva è, comunque, necessaria per rispondere alle domande sulla presenza o frequenza del sintomo (“Quante volte ha avuto dolore alle ginocchia questa settimana?”) o sulla sua intensità (“Quanto dolore alle ginocchia ha avuto questa settimana?”). La raccolta dei PROs si basa, di solito, su una analisi retrospettiva della presenza, frequenza o severità dei sintomi specifici di malattia. Alcuni aspetti multidimensionali, tuttavia, quali la correlazione stato di salute-qualità della vita o lo stato di benessere, dipendono dal contesto e dal momento in cui vengono valutati. Le sottocomponenti della qualità di vita o del benessere soggettivo rappresentano la somma di più esperienze quotidiane e momentanee vissute dal paziente. La rievocazione dell’accumulo di più momenti o esperienze, pertanto, può portare a sottostimare l’entità della sintomatologia o dell’evento. Per la raccolta dei dati PROs, tradizionalmente, vengono utilizzati diari ad intervalli di tempo prefissati, al fine di ridurre al minimo i “bias” da richiamo dell’evento. Nel corso degli anni sono stati sviluppati nuovi metodi per acquisire i PROs, con una minore distorsione e migliore qualità dei dati rispetto ai diari in versione cartacea. Tali nuove metodologie, che si basano sul concetto denominato “Ecological Momentary Assessment” (EMA), consente la raccolta dei dati in tempo reale nel corso delle attività quotidiane. Tale tipologia di valutazione permette di attuare delle strategie di campionamento focalizzate su una prospettiva unica ed in riferimento a delle esperienze vissute in tempo reale dal paziente. Un potenziale elemento di distorsione dei dati PROs è rappresentato dalla reattività dello strumento. La reattività, definita come il grado in cui l’intensità, la frequenza e / o la qualità di una variabile cambia in funzione della osservazione o valutazione, dipende, a sua volta, da due elementi: dal contenuto della stessa valutazione e dalla metodologia utilizzata per raccogliere i dati. I quesiti e le scale dei questionari di valutazione della qualità della vita, nel pieno rispetto del modello teorico della “item-measurement theory”, sono concepiti per l’auto-somministrazione, l’intervista telefonica, l’invio postale o la sommnistrazione mediante strumenti informatici.
Autosomministrazione durante l’accesso alla struttura sanitaria
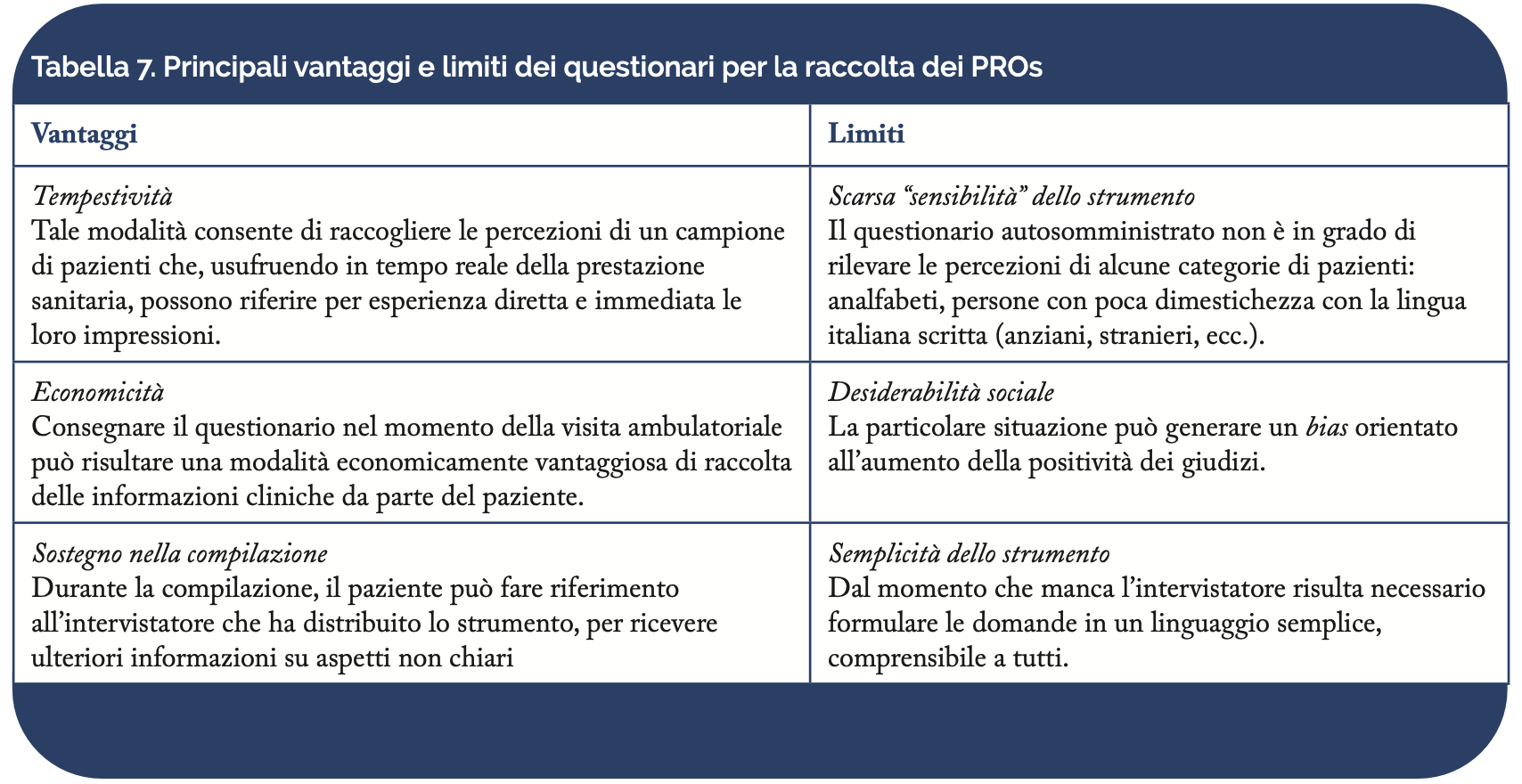
I questionari vengono somministrati, in versione cartacea, nel momento di contatto con il clinico, quando il paziente si reca fisicamente presso la struttura sanitaria. Il questionario viene consegnato personalmente al paziente e consente una immediata ed economica raccolta di informazioni (Tabella 7).
Un intervistatore pone le domande del questionario a un intervistato così come sono scritte, rispettandone l’ordine e il fraseggio, e prende nota delle risposte. La credibilità, la riconoscibilità dell’intervistatore, così come la formazione e l’addestramento al suo ruolo possono influenzare la qualità delle risposte e, pertanto, è fondamentale che esso mantenga lo stesso atteggiamento interpersonale con tutti gli intervistati e per tutte le domande e non commenti le risposte.
Intervista telefonica
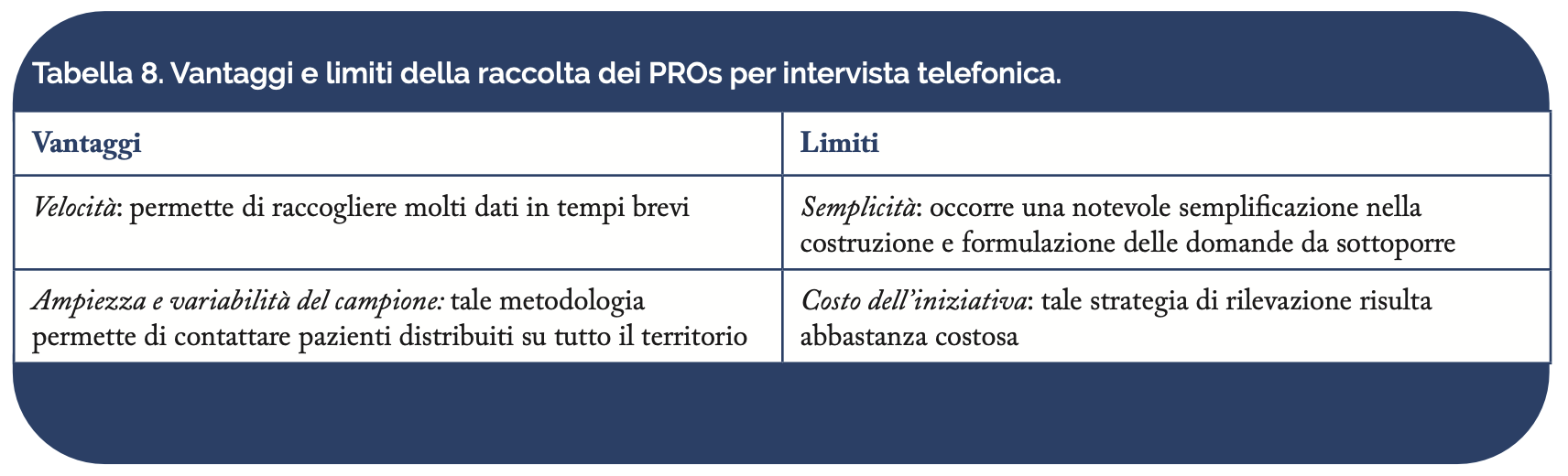
Un’ulteriore modalità di intervista, attuata nel contesto della valutazione degli aspetti correlati allo stato di salute, è quella telefonica. L’intervista telefonica si usa, solitamente, quando sono disponibili i dati personali di un campione di cittadini che sono contattati telefonicamente, a cui vengono poste le domande e registrate le risposte. Tale modalità consente la raccolta di molti dati su ampie popolazioni in tempi relativamente brevi (Tabella 8).
Somministrazione postale
La somministrazione del questionario per posta prevede, di solito, una lettera di presentazione. La spedizione dei questionari dovrebbe avvenire entro una-due settimane dalla valutazione clinica basale, per evitare sostanziali difformità di valutazione (variazioni del contesto). Tale modalità presenta vantaggi e limiti (Tabella 9).
Somministrazione mediante strumenti informatici
Una terza modalità di somministrazione è quella dell’intervista tramite strumenti informatizzati. L’attuale disponibilità di diari elettronici (eDiary) e la realizzazione di idonee piattaforme hardware e software hanno aperto nuovi scenari sulla possibile applicabilità di sistemi di monitoraggio informatizzato per la raccolta dei PROs. L’adozione di specifici accorgimenti nella realizzazione dei dispositivi di rilevazione elettronica, come ad esempio l’impiego di schermi o totem con tecnologia “touch screen”, si riflettono in una serie di vantaggi pratici (Tabella 10), che ha reso la raccolta delle informazioni cliniche più facili e comprensibili per il paziente, con conseguente miglioramento della compliance nei confronti dello strumento elettronico, rispetto al corrispettivo metodo cartaceo (diari o questionari tradizionali).
L’affermarsi del concetto di database quale strumento di monitoraggio del malato reumatico, lo sviluppo ed il largo l’impiego in campo reumatologico degli strumenti di valutazione dell’impatto della malattia sullo stato globale di salute e l’avvento delle più recenti tecnologie hardware e software a basso costo hanno condizionato nell’ultimo decennio in maniera sostanziale i tradizionali percorsi diagnostico-valutativi ed il processo decisionale del medico. Gli sviluppi tecnologici, in particolare, hanno reso sempre più possibile la raccolta di informazioni precise, aggiornate e “in tempo reale” relative allo stato di salute del paziente.
Punti chiave
- La misura della qualità della vita nelle malattie muscoloscheletriche è considerata elemento di fondamentale importanza, non solo in ambito valutativo, ma anche in chiave prognostica.
- Il termine qualità di vita correlata alla salute (HRQoL) si riferisce genericamente al benessere (emotivo, sociale e fisico) di un individuo ed alla sua capacità di adempiere ai compiti della vita quotidiana in maniera soddisfacente.
- Le due principali tipologie di studi sulla qualità della vita sono rappresentati da: (a) studi descrittivi finalizzati ad una misurazione analitica della qualità della vita e privi di implicazioni economiche; (b) studi finalizzati alla misurazione della qualità della vita mediante la tecnica della “utilità” e connessi ad analisi economiche sui costi verso i benefici.
- Gli strumenti per la valutazione della qualità della vita, prima di poter essere utilizzati, devono passare al vaglio di rigorosissimi metodi di validazione che ne garantiscono la validità, la consistenza interna e la riproducibilità e la sensibilità.
Bibliografia
- D’Angelo S, Malavolta N, Scambi C, Salvarani C, Caso F, Tirri E, Ramonda R, Quarta L, Erre GL, Riva M, Buono R, Furini F, Grembiale RD, Lomater C, Cantini F, Maio T, Chimenti MS, Scrivo R, Salaffi F, Caporali RF, Volpe P, Gualberti G, Marando F, Marchesoni A. Quality of life and therapeutic management of axial spondyloarthritis patients in Italy: a 12-month prospective observational study. Clin Exp Rheumatol. 2021 Jan 6. Epub ahead of print.
- Favero M, Ometto F, Salaffi F, Belluzzi E, Ortolan A, Lorenzin M, Felicetti M, Punzi L, Ndosi M, Ramonda R. Validation of the Italian Version of the Educational Needs Assessment Tool in Rheumatoid Arthritis Patients and Factors Associated with Educational Needs. J Pers Med. 2020 1;10(4):150.
- Salaffi F, Di Carlo M, Carotti M, Ceccarelli L, Farah S, Marotto D, Giorgi V, Sarzi-Puttini P. Predictive validity of the 5-item Compliance Questionnaire for Rheumatology (CQR5) in detecting poor adherence of patients with rheumatoid arthritis to biological medication. Arthritis Res Ther. 2020 29;22(1):227.
- Salaffi F, Di Carlo M, Bazzichi L, Atzeni F, Govoni M, Biasi G, Di Franco M, Mozzani F, Gremese E, Dagna L, Batticciotto A, Fischetti F, Giacomelli R, Guiducci S, Guggino G, Bentivegna M, Gerli R, Salvarani C, Bajocchi G, Ghini M, Iannone F, Giorgi V, Farah S, Cirillo M, Bonazza S, Barbagli S, Gioia C, Santilli D, Capacci A, Cavalli G, Carubbi F, Nacci F, Riccucci I, Sinigaglia L, Masullo M, Polizzi BM, Cutolo M, Sarzi-Puttini P. Definition of fibromyalgia severity: findings from a cross-sectional survey of 2339 Italian patients. Rheumatology (Oxford). 2020 Aug 13:keaa355.
- Salaffi F, Di Carlo M, Carotti M, Farah S, Giovagnoni A. Frailty prevalence according to the Survey of Health, Ageing and Retirement in Europe-Frailty Instrument (SHARE-FI) definition, and its variables associated, in patients with symptomatic knee osteoarthritis: findings from a cross-sectional study. Aging Clin Exp Res. 2020 Jul 30.
- Benfaremo D, Luchetti MM, Di Carlo M, Laganà B, Picchianti-Diamanti A, Carubbi F, Pica R, Chimenti MS, Lorenzetti R, Scolieri P, Bruzzese V, Benedetti A, Ramonda R, Giacomelli R, Salaffi F, Gabrielli A; GRADES-IBD Study Group. Multicenter Validation of the DETAIL Questionnaire for the Screening of Spondyloarthritis in Patients With Inflammatory Bowel Diseases. J Rheumatol. 2021;48(2):179-187.
- Salaffi F, Farah S, Di Carlo M. Frailty syndrome in rheumatoid arthritis and symptomatic osteoarthritis: an emerging concept in rheumatology. Acta Biomed. 2020 May 11;91(2):274-296.
- Salaffi F, Di Carlo M, Farah S, Atzeni F, Buskila D, Ablin JN, Häuser W, Sarzi-Puttini P. Diagnosis of fibromyalgia: comparison of the 2011/2016 ACR and AAPT criteria and validation of the modified Fibromyalgia Assessment Status. Rheumatology (Oxford). 2020 Oct 1;59(10):3042-3049.
- Salaffi F, Di Carlo M, Farah S, Carotti M. Adherence to subcutaneous anti- TNFα agents in patients with rheumatoid arthritis is largely influenced by pain and skin sensations at the injection site. Int J Rheum Dis. 2020;23(4):480- 487.
- Salaffi F, Farah S, Di Carlo M, Sinigaglia L, Galeazzi M, Gerli R, Sonnati M, Giorgi V, Sarzi-Puttini P, Masullo M; Italian Society of Rheumatology (SIR) and Ministero della Salute – Direzione Generale della Programmazione Sanitaria, Roma, Italy.. The Italian Fibromyalgia Registry: a new way of using routine real-world data concerning patient-reported disease status in healthcare research and clinical practice. Clin Exp Rheumatol. 2020;38 Suppl 123(1):65- 71.
- Di Carlo M, Tardella M, Di Matteo A, Beci G, De Angelis R, Salaffi F. A proposal on how to assess the weight of the subjective components of the DAPSA in patients with psoriatic arthritis and comorbid fibromyalgia syndrome. Clin Exp Rheumatol. 2020;38 Suppl 123(1):60-64.
- Salaffi F, Di Carlo M, Farah S, Carotti M. The Comprehensive Rheumatologic Assessment of Frailty (CRAF): development and validation of a multidimensional frailty screening tool in patients with rheumatoid arthritis. Clin Exp Rheumatol. 2020;38(3):488-499.
- Salaffi F, Farah S, Beci G, Schettino M, Carotti M, Di Carlo M. Development and validation of the SImple FIbromyalgia Screening questionnaire for improving the recognition of fibromyalgia in daily practice. Clin Exp Rheumatol. 2020;38 Suppl 123(1):9-16.
- Salaffi F, Di Carlo M, Carotti M, Farah S, Ciapetti A, Gutierrez M. The impact of different rheumatic diseases on health-related quality of life: a comparison with a selected sample of healthy individuals using SF-36 questionnaire, EQ-5D and SF-6D utility values. Acta Biomed. 2019 15;89(4):541-557.
- Salaffi F, Carotti M, Di Donato E, Di Carlo M, Luchetti MM, Ceccarelli L, Giovagnoni A. Preliminary validation of the Simplified Psoriatic Arthritis Radiographic Score (SPARS). Skeletal Radiol. 2019;48(7):1033-1041.
- Salaffi F, Di Carlo M, Carotti M, Farah S. Validity and interpretability of the QuickDASH in the assessment of hand disability in rheumatoid arthritis. Rheumatol Int. 2019;39(5):923-932.
- Salaffi F, Di Carlo M, Carotti M, Farah S. The Patient-Reported Outcomes Thermometer-5-Item Scale (5T-PROs): Validation of a New Tool for the Quick Assessment of Overall Health Status in Painful Rheumatic Diseases. Pain Res Manag. 2018 23;2018:3496846.
- Salaffi F, Carotti M, Di Carlo M, Tardella M, Lato V, Becciolini A, Favalli EG, Giovagnoni A. The Expanded Risk Score in Rheumatoid Arthritis (ERS-RA): performance of a disease-specific calculator in comparison with the traditional prediction scores in the assessment of the 10-year risk of cardiovascular disease in patients with rheumatoid arthrit. Swiss Med Wkly. 2018 22;148:w14656.
- Salaffi F, Di Carlo M, Carotti M, Sarzi-Puttini P. The subjective components of the Disease Activity Score 28-joints (DAS28) in rheumatoid arthritis patients and coexisting fibromyalgia. Rheumatol Int. 2018;38(10):1911-1918.
- Di Carlo M, Luchetti MM, Benfaremo D, Di Donato E, Mosca P, Maltoni S, Benedetti A, Gabrielli A, Grassi W, Salaffi F. The DETection of Arthritis in Inflammatory boweL diseases (DETAIL) questionnaire: development and preliminary testing of a new tool to screen patients with inflammatory bowel disease for the presence of spondyloarthritis. Clin Rheumatol. 2018;37(4):1037-1044.
- Salaffi F, Di Carlo M, Luchetti MM, Di Donato E, Campanati A, Benfaremo D, Nicolini M, Carotti M, Giacchetti A, Ganzetti G, Bugatti L, Gabrielli A, Offidani AM. A validation study of the Simple Psoriatic Arthritis Screening (SiPAS) questionnaire to screen psoriasis patients for psoriatic arthritis. Clin Exp Rheumatol. 2018;36(1):127-135.
- Salaffi F, Di Carlo M, Iannone F, Fedele AL, Epis OM, Pellerito R, Foti R, Passiu G, Punzi L, Furini F, Sarzi-Puttini P, Carletto A, Gremese E, Lapadula G, Ferraccioli G. The UltraSound-CLinical ARthritis Activity (US-CLARA) index: Properties of a new composite disease activity index for rheumatoid arthritis. Semin Arthritis Rheum. 2018;47(5):619-629.
- Salaffi F, Di Carlo M, Vojinovic J, Tincani A, Sulli A, Soldano S, Andreoli L, Dall’Ara F, Ionescu R, SimićPašalićK, Balčune I, Ferraz-Amaro I, Tlustochowicz M, ButrimienėI, Punceviciene E, Toroptsova N, Grazio S, Morović– Vergles J, Masaryk P, Otsa K, Bernardes M, Boyadzhieva V, Cutolo M. Validity of the rheumatoid arthritis impact of disease (RAID) score and definition of cut- off points for disease activity states in a population-based European cohort of patients with rheumatoid arthritis. Joint Bone Spine. 2018;85(3):317-322.
- Vojinovic J, Tincani A, Sulli A, Soldano S, Andreoli L, Dall’Ara F, Ionescu R, Pasalic KS, Balcune I, Ferraz-Amaro I, Tlustochowicz M, Butrimiene I, Punceviciene E, Toroptsova N, Grazio S, Morovic-Vergles J, Masaryk P, Otsa K, Bernardes M, Boyadzhieva V, Salaffi F, Cutolo M. European multicentre pilot survey to assess vitamin D status in rheumatoid arthritis patients and early development of a new Patient Reported Outcome questionnaire (D-PRO). Autoimmun Rev. 2017;16(5):548-554.
- Lapadula G, Marchesoni A, Salaffi F, Ramonda R, Salvarani C, Punzi L, Costa L, Caso F, Simone D, Baiocchi G, Scioscia C, Di Carlo M, Scarpa R, Ferraccioli G. Evidence-based algorithm for diagnosis and assessment in psoriatic arthritis: results by Italian DElphi in psoriatic Arthritis (IDEA). Reumatismo. 2016 16;68(3):126-136.
- Di Carlo M, Becciolini A, Lato V, Crotti C, Favalli EG, Salaffi F. The 12-item Psoriatic Arthritis Impact of Disease Questionnaire: Construct Validity, Reliability, and Interpretability in a Clinical Setting. J Rheumatol. 2017;44(3):279- 285.
- Salaffi F, Di Carlo M, Bugatti L, Lato V, Nicolini M, Carotti M. Development and pilot-testing of a new tool to screen psoriasis patients for the presence of psoriatic arthritis: the Simple Psoriatic Arthritis Screening (SiPAS) questionnaire. J Eur Acad Dermatol Venereol. 2017;31(3):e167-e169.
- Di Carlo M, Lato V, Carotti M, Salaffi F. Clinimetric properties of the ASAS health index in a cohort of Italian patients with axial spondyloarthritis. Health Qual Life Outcomes. 2016 17;14:78.
- Salaffi F, Di Carlo M, Carotti M, Farah S, Gutierrez M. The Psoriatic Arthritis Impact of Disease 12-item questionnaire: equivalence, reliability, validity, and feasibility of the touch-screen administration versus the paper- and-pencil version. Ther Clin Risk Manag. 2016 21;12:631-42..
- Ramonda R, Marchesoni A, Carletto A, Bianchi G, Cutolo M, Ferraccioli G, Fusaro E, De Vita S, Galeazzi M, Gerli R, Matucci-Cerinic M, Minisola G, Montecucco C, Pellerito R, Salaffi F, Paolazzi G, Sarzi-Puttini P, Scarpa R, Bagnato G, Triolo G, Valesini G, Punzi L, Olivieri I; ATLANTIS study group. Patient-reported impact of spondyloarthritis on work disability and working life: the ATLANTIS survey. Arthritis Res Ther. 2016 1;18:78.
- Salaffi F, Carotti M, Gutierrez M, Di Carlo M, De Angelis R. Patient Acceptable Symptom State in Self-Report Questionnaires and Composite Clinical Disease Index for Assessing Rheumatoid Arthritis Activity: Identification of Cut-Off Points for Routine Care. Biomed Res Int. 2015;2015:930756.
- Salaffi F, Ciapetti A, Carotti M, Gasparini S, Citera G, Gutierrez M. Construct validity and responsiveness of the simplified version of Ankylosing Spondylitis Disease Activity Score (SASDAS) for the evaluation of disease activity in axial spondyloarthritis. Health Qual Life Outcomes. 2014 22;12:129.
- Franchignoni F, Salaffi F, Ciapetti A, Giordano A. Searching for optimal rating scales in the Bath Ankylosing Spondylitis Functional Index (BASFI) and Bath Ankylosing Spondylitis Disease Activity Index (BASDAI). Rheumatol Int. 2014 Feb;34(2):171-3.
- Salaffi F, Franchignoni F, Giordano A, Ciapetti A, Sarzi- Puttini P, Ottonello M. Psychometric characteristics of the Italian version of the revised Fibromyalgia Impact Questionnaire using classical test theory and Rasch analysis. Clin Exp Rheumatol. 2013;31(6 Suppl 79):S41-9
- Salaffi F, Franchignoni F, Giordano A, Ciapetti A, Gasparini S, Ottonello M; “NEW INDICES” Study Group. Classical test theory and Rasch analysis validation of the Recent-Onset Arthritis Disability questionnaire in rheumatoid arthritis patients. Clin Rheumatol. 2013;32(2):211-7
- Franchignoni F, Salaffi F, Giordano A, Carotti M, Ciapetti A, Ottonello M. Rasch analysis of the 22 knee injury and osteoarthritis outcome score-physical function items in Italian patients with knee osteoarthritis. Arch Phys Med Rehabil. 2013;94(3):480-7.
- Salaffi F, Ciapetti A, Gasparini S, Carotti M, Bombardieri S; New Indices study group. The comparative responsiveness of the patient self-report questionnaires and composite disease indices for assessing rheumatoid arthritis activity in routine care. Clin Exp Rheumatol. 2012 Nov-Dec;30(6):912-21
- Iannuccelli C, Sarzi-Puttini P, Atzeni F, Cazzola M, di Franco M, Guzzo MP, Bazzichi L, Cassisi GA, Marsico A, Stisi S, Salaffi F. Psychometric properties of the Fibromyalgia Assessment Status (FAS) index: a national web-based study of fibromyalgia. Clin Exp Rheumatol. 2011;29(6 Suppl 69):S49-54.
- Salaffi F, Carotti M, Ciapetti A, Gasparini S, Grassi W. A comparison of utility measurement using EQ-5D and SF- 6D preference-based generic instruments in patients with rheumatoid arthritis. Clin Exp Rheumatol. 2011;29(4):661- 71
- Salaffi F, Ciapetti A, Gasparini S, Migliore A, Scarpellini M, Corsaro SM, Laganà B, Mozzani F, Varcasia G, Pusceddu M, Castriotta M, Serale F, Maier A, Foti R, Scarpa R, Bombardieri S; NEW INDICES Study Group. Comparison of the Recent-Onset Arthritis Disability questionnaire with the Health Assessment Questionnaire disability index in patients with rheumatoid arthritis. Clin Exp Rheumatol. 2010;28(6):855-65.
- Salaffi F, Migliore A, Scarpellini M, Corsaro SM, Laganà B, Mozzani F, Varcasia G, Pusceddu M, Pomponio G, Romeo N, Maier A, Foti R, Scarpa R, Gasparini S, Bombardieri S. Psychometric properties of an index of three patient reported outcome (PRO) measures, termed the CLinical ARthritis Activity (PRO- CLARA) in patients with rheumatoid arthritis. The NEW INDICES study. Clin Exp Rheumatol. 2010 28(2):186-200.
- Salaffi F, Vaccaro CM, Manacorda T, Pardini L, Coletta V, Montecucco C. La qualità della vita dei pazienti con artrite reumatoide: valutazione mediante la versione italiana del questionario Arthritis Impact Measurement Scales 2 (AIMS2) [Health-related quality of life in patients with rheumatoid arthritis: assessment by a Italian version of the Arthritis Impact Measurement Scales, Version 2 (AIMS2)]. Reumatismo. 2010;62(1):12-33.
- Salaffi F, Sarzi-Puttini P, Ciapetti A, Atzeni F. Assessment instruments for patients with fibromyalgia: properties, applications and interpretation. Clin Exp Rheumatol. 2009 27(5 Suppl 56):S92-105.
- Salaffi F, Sarzi-Puttini P, Girolimetti R, Atzeni F, Gasparini S, Grassi W. Health-related quality of life in fibromyalgia patients: a comparison with rheumatoid arthritis patients and the general population using the SF-36 health survey. Clin Exp Rheumatol. 2009 Sep-Oct;27(5 Suppl 56):S67- 74.
- Salaffi F, Sarzi-Puttini P, Girolimetti R, Gasparini S, Atzeni F, Grassi W. Development and validation of the self-administered Fibromyalgia Assessment Status: a disease-specific composite measure for evaluating treatment effect. Arthritis Res Ther. 2009;11(4):R125
- Salaffi F, Carotti M, Gasparini S, Intorcia M, Grassi W. The health-related quality of life in rheumatoid arthritis, ankylosing spondylitis, and psoriatic arthritis: a comparison with a selected sample of healthy people. Health Qual Life Outcomes. 2009 18;7:25.
- De Angelis R, Salaffi F, Grassi W. Health-related quality of life in primary Raynaud phenomenon. J Clin Rheumatol. 2008;14(4):206-10
- Salaffi F, Malavolta N, Cimmino MA, Di Matteo L, Scendoni P, Carotti M, Stancati A, Mulé R, Frigato M, Gutierrez M, Grassi W; Italian Multicentre Osteoporotic Fracture (IMOF) Study Group. Validity and reliability of the Italian version of the ECOS-16 questionnaire in postmenopausal women with prevalent vertebral fractures due to osteoporosis. Clin Exp Rheumatol. 2007;25(3):390-403.
- Salaffi F, Cimmino MA, Malavolta N, Carotti M, Di Matteo L, Scendoni P, Grassi W; Italian Multicentre Osteoporotic Fracture Study Group. The burden of prevalent fractures on health-related quality of life in postmenopausal women with osteoporosis: the IMOF study. J Rheumatol. 2007;34(7):1551-60.
- Salaffi F, Stancati A, Grassi W. Reliability and validity of the Italian version of the Chronic Pain Grade questionnaire in patients with musculoskeletal disorders. Clin Rheumatol. 2006 Sep;25(5):619-31. 51: Salaffi F, De Angelis R, Stancati A, Grassi W; MArche Pain; Prevalence INvestigation Group (MAPPING) study. Health-related quality of life in multiple musculoskeletal conditions: a cross-sectional population based epidemiological study. II. The MAPPING study. Clin Exp Rheumatol. 2005;23(6):829-39.
- Salaffi F, Stancati A, Procaccini R, Cioni F, Grassi W. Valutazione del ritmo circadiano del dolore e della rigidità nelle malattie reumatiche secondo la metodica EMA (Ecologic Momentary Assessment): compliance del paziente con un diario elettronico [Assessment of circadian rhythm in pain and stiffness in rheumatic diseases according the EMA (Ecologic Momentary Assessment) method: patient compliance with an electronic diary]. Reumatismo. 2005;57(4):238-49.
- Salaffi F, Carotti M, Stancati A, Grassi W. Health-related quality of life in older adults with symptomatic hip and knee osteoarthritis: a comparison with matched healthy controls. Aging Clin Exp Res. 2005;17(4):255-63.
- Salaffi F, Stancati A, Neri R, Grassi W, Bombardieri S. Measuring functional disability in early rheumatoid arthritis: the validity, reliability and responsiveness of the Recent- Onset Arthritis Disability (ROAD) index. Clin Exp Rheumatol. 2005;23(5 Suppl 39):S31-42.
- Salaffi F, Stancati A, Silvestri A, Carotti M, Grassi W. Validazione delle versioni italiane del Bath Ankylosing Spondylitis Functional Index (BASFI) e del Dougados Functional Index (DFI) in pazienti con spondilite anchilosante [Validation of the Italian versions of the Bath Ankylosing Spondylitis Functional Index (BASFI) and the Dougados Functional Index (DFI) in patients with ankylosing spondylitis]. Reumatismo. 2005;57(3):161-73.
- Salaffi F, Bazzichi L, Stancati A, Neri R, Cazzato M, Consensi A, Grassi W, Bombardieri S. Development of a functional disability measurement tool to assess early arthritis: the Recent-Onset Arthritis Disability (ROAD) questionnaire. Clin Exp Rheumatol. 2005;23(5):628-36.
- Salaffi F, Stancati A, Carotti M, Lorenzetti R, Grassi W. Impatto sulla qualità della vita delle fratture vertebrali in donne in età postmenopausale affette da osteoporosi. Validità della versione italiana del mini-Osteoporosis Quality of Life Questionnaire [The impact of vertebral fractures on quality of life in postmenopausal women with osteoporosis. Validity of the Italian version of mini-Osteoporosis Quality of Life Questionnaire.]. Reumatismo. 2005;57(2):83-96.
- Salaffi F, Carotti M, Grassi W. Health-related quality of life in patients with hip or knee osteoarthritis: comparison of generic and disease-specific instruments. Clin Rheumatol. 2005 Feb;24(1):29-37
- Salaffi F, Silveri F, Stancati A, Grassi W. Development and validation of the osteoporosis prescreening risk assessment (OPERA) tool to facilitate identification of women likely to have low bone density. Clin Rheumatol. 2005 Jun;24(3):203-11.
- Doria A, Rinaldi S, Ermani M, Salaffi F, Iaccarino L, Ghirardello A, Zampieri S, Della Libera S, Perini G, Todesco S. Health-related quality of life in Italian patients with systemic lupus erythematosus. II. Role of clinical, immunological and psychological determinants. Rheumatology. 2004;43(12):1580-6.
- Rinaldi S, Doria A, Salaffi F, Ermani M, Iaccarino L, Ghirardello A, Zampieri S, Sarzi-Puttini P, Gambari PF, Perini G. Health-related quality of life in Italian patients with systemic lupus erythematosus. I. Relationship between physical and mental dimension and impact of age. Rheumatology (Oxford). 2004;43(12):1574-9.
- Salaffi F, Stancati A, Silvestri CA, Ciapetti A, Grassi W. Minimal clinically important changes in chronic musculoskeletal pain intensity measured on a numerical rating scale. Eur J Pain. 2004;8(4):283-91.
- Salaffi F, Leardini G, Canesi B, Mannoni A, Fioravanti A, Caporali R, Lapadula G, Punzi L; GOnorthrosis and Quality Of Life Assessment (GOQOLA). Reliability and validity of the Western Ontario and McMaster Universities (WOMAC) Osteoarthritis Index in Italian patients with osteoarthritis of the knee. Osteoarthritis Cartilage. 2003;11(8):551-60
- Salaffi F, Stancati A, Carotti M. Responsiveness of health status measures and utility-based methods in patients with rheumatoid arthritis. Clin Rheumatol. 2002;21(6):478-87.
- Salaffi F, Piva S, Barreca C, Cacace E, Ciancio G, Leardini G, Mannoni A, Minari C, Occhi P, Pianon M, Punzi L, Re KA, Scarpa R, Sulli A, Troise-Rioda W. Validation of an Italian version of the arthritis impact measurement scales 2 (ITALIAN-AIMS2) for patients with osteoarthritis of the knee. Gonarthrosis and Quality of Life Assessment (GOQOLA) Study Group. Rheumatology (Oxford). 2000;39(7):720-7.
- Salaffi F, Peroni M, Ferraccioli GF. Discriminating ability of composite indices for measuring disease activity in rheumatoid arthritis: a comparison of the Chronic Arthritis Systemic Index, Disease Activity Score and Thompson’s articular index. Rheumatology (Oxford). 2000 Jan;39(1):90-6.